Фаза десквамации эндометрия что это
В этой фазе цикла слизистая оболочка матки, особенно ее функциональная зона, в значительной мере переполнена кровью. В связи с расширением капилляров, по которым вместе с кровью поступает материал, необходимый для образования секрета, постепенно наступает стаз (застой) крови в сосудах слизистой оболочки с его последующей транссудацией в окружающую ткань собственной пластинки. В результате этого слизистая оболочка, насыщенная кровяным транссудатом и слизистым секретом желез, набухает (приобретает отечную консистенцию) и размягчается, благодаря чему возникают благоприятные условия для нидации зародыша.
Во время фазы секреции в яичнике функционирует желтое тело, которое к концу фазы начинает постепенно дегенерировать и подвергаться обратному развитию. В этот период яйцевая клетка, выброшенная из граафова фолликула, передвигается по яйцеводу; в случае оплодотворения она нидирует в подготовленную таким образом слизистую оболочку матки. Фаза секреции, начавшись с 14—15-го дня менструального цикла, продолжается до 28-го дня включительно.
Фаза десквамации (отторжения — menstruum). В том случае, если оплодотворения и нидации яйцевой клетки к слизистой оболочке матки не произошло, желтое тело постепенно гибнет, а функциональная зона слизистой оболочки, перенасыщенная кровью в фазе секреции, становится ишемической, с недостаточным кровонаполнением, из-за сокращения сосудов и затрудненного притока крови; в связи с этим она все больше пропитывается жидкостью и размягчается при одновременной дегенерации ткани.
Таким образом распадающаяся, отслаивающаяся и дегенерирующаяся ткань функционального слоя слизистой оболочки, пропитанная кровяным транссудатом и секретами, постепенно в виде кусков, вместе с поверхностным эпителиальным слоем отторгается от базального слоя (decidua menstruationis). Отторженная слизистая вместе с кровью, изливающейся из нарушенных сосудов, смешивается с секретами маточных желез и выделяется из матки через влагалище.
Такое менструальное отделение крови (менструация) длится обычно четыре дня, то есть, начиная с первого дня менструального цикла и кончая четвертым днем включительно.
В яичнике в это время продолжается обратное развитие желтого тела, и начинает созревать новый фолликул, что представляет собой вступление к повторному восстановлению нарушенной слизистой оболочки.
Фаза регенерации (postmenstruum). После десквамации, отторжения функционального слоя слизистой оболочки матки поверхность ее полости покрыта одним лишь обнаженным базальным слоем слизистой; в это время базальный слой очень тонок, в нем располагаются основания маточных желез. В фазе регенерации, благодаря размножению эпителиальных клеток этих остатков желез, происходит регенерация поверхностного эпителия, который затем очень быстро покрывает раневую внутреннюю поверхность маточной полости. Сразу же после этого следует новая фаза пролиферации следующего менструального цикла.
Фаза регенерации заканчивается на 5-ый день менструального цикла.
Под регулярным двадцативосьмидневным повторением маточного цикла и менструального отделения крови подразумеваются средние сроки в рамках биологических вариаций. Менструальный цикл может подвергаться отдельным индивидуальным колебаниям; его отклонения как в отношении общей длительности всего цикла, так и в отношении продолжительности его отдельных фаз по сравнению со средними сроками (от 24 до 32 дней) еще не означают ничего ненормального или патологического, если они не связаны с иными нарушениями или же затруднениями. Таким образом, если менструация не длится в течение четырех дней, то это еще не является доказательством какого-либо нарушения.
Нередко наблюдаются трех- или же пятидневные менструальные отделения крови.
Нерегулярные или избыточные маточные кровотечения
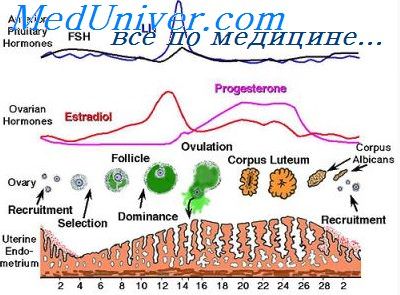
Во время фолликулярной фазы (1 фаза) менструального цикла под действием эстрогенов толщина эндометрия увеличивается. На гистологическом уровне этот процесс проявляется возрастанием количества митозов в железах, то есть происходит рост эндометрия. Во время лютеиновой фазы (2 фаза), продуцируемый желтым телом прогестерон останавливает рост эндометрия, вызывает в нем секреторную трансформацию, обеспечивая условия для имплантации оплодотворенной яйцеклетки. В конце менструального цикла, если не наступила беременность, вследствие регресса желтого тела в крови падают уровни женских половых гормонов, что приводит к началу менструальных кровотечений.
Начало и завершение нормального менструального кровотечения требует четкого взаимодействия между гормональными влияниями и эндометрием. Во время лютеиновой фазы менструального цикла эндометрий состоит из трех слоев: базального, губчатого слоя и компактного слоя. Базальный слой находится на границе между миометрием и эндометрием и именно из него в каждом новом цикле обновляется эндометрий. Губчатый слой, следующий после базального, является самым толстым слоем, занимающим половину всей толщины эндометрия во второй фазе цикла. В губчатом слое располагаются спиральные артерии.
Сосудистая структура эндометрия является продолжением сосудов миометрия. Аркуатные артерии миометрия, разветвляясь, формируют радиальные и базальные артерии, которые начинают извиваться и создают так называемые спиральные артерии, проникающие в эндометрий. Спиральные артерии, в отличие от базальных, чувствительны к колебаниям эстрогенов и прогестерона, что обеспечивает процесс десквамации функционального слоя эндометрия вследствие вазоконстрикции, приводящей к ишемии и некрозу. После завершения десквамации начинается регенерация базальных артерий. На микроскопическом уровне в этом процессе выделяют 4 стадии: а) разрушение базальной мембраны; б) миграция эндотелиальных клеток; в) пролиферация эндотелиальных клеток и г) формирование капилляра. В процессе деградации базальной мембраны специфические ферменты (стромелизин, коллагеназа и др.) разрушают элементы экстацеллюлярного матрикса. Затем эндотелиальные клетки мигрируют в конец сосуда, чему способствуют среда, богатая коллагеном I и III типа и стимулирующее действие bFGF. Дальнейшая пролиферация эндотелиальных клеток и формирование просвета, вероятно, тоже зависят от компонентов экстацеллюлярного матрикса.
Таким образом, механизм, посредством которого осложнения беременности могут привести к появлению маточного кровотечения, становится очевидным. Процесс имплантации эмбриона включает в себя инвазию трофобласта в эндометрий, в чем существенную роль играет развитие локальной сосудистой сети в эндометрии, обеспечивающей условия для дальнейшего протекания беременности. В случаях, когда беременность по той или иной причине начинает прерываться, материнские сосуды открываются в полость матки, что приводит к развитию кровотечения.
Опухоли матки вызывают кровотечение за счет разрушения нормальной целостности структуры эндометрия. Маточные кровотечения, вызванные эндометритом, являются следствием разрушения сосудов и желез эндометрия веществами, продуцирующимися при воспалении.
Первым этапом в формировании тромба является агрегация тромбоцитов, поэтому любые заболевания, сопровождающиеся нарушением агрегации тромбоцитов (тромбофилии, нарушения в системе гемостаза, тромбоцитопеническая пурпура и др.), могут привести к маточным кровотечениям.
Среди гормональных нарушений, приводящих к патологическим маточным кровотечениям, ведущее место занимает ановуляция. Суть ановуляторных кровотечений заключается в длительной стимуляции эндометрия эстрогенами в отсутствии прогестерона, что приводит к избыточному росту эндометрия и периодическому его отторжению за счет дистрофических процессов в поверхностных слоях.
Гормональные нарушения, приводящие к патологическим маточным кровотечениям
Причин для нарушения овуляции множество. В большинстве случаев первые менструальные циклы после менархе – ановуляторные, однако, в дальнейшем при нормальном функционировании всех систем, циклы становятся овуляторными. В норме, 2-3 года после менархе менструальный цикл может быть ановуляторным с характерной этому состоянию нерегулярностью. Среди наиболее распространенных причин, препятствующих овуляции на ранних этапах можно выделить нарушение функции гипоталамо-гипофизарного комплекса вследствие перенесенных нейроинфекций, травм, пороков развития, эндокринопатий, а также другие причины, обусловленные недостаточной массой тела и психическими факторами и др.
Наибольший риск развития гиперпластических процессов эндометрия и карцином эндометрия (рака) наблюдается у женщин пременопаузального возраста в особенности на фоне повышенной массы тела. Предполагается, что внеяичниковый синтез эстрогенов в жировой клетчатке, за счет ферментации андрогенов в эстрогены, суммируясь с эстрогенами яичникового происхождения, приводит к усилению пролиферативных процессов в эндометрии, что в условиях отсутствия адекватной продукции прогестерона создает фон для формирования гиперплазии. Однако, помимо гиперэстрогении и недостаточности прогестерона необходимы другие факторы для развития гиперпластического процесса. Интересно, почему у молодых девушек с повышенной массой тела и ановуляторным менструальным циклом гиперпластические процессы эндометрия развиваются крайне редко? Принимая во внимание результаты нескольких последних исследований, вероятнее всего большую роль в формировании гиперпластических процессов эндометрия играет хронический эндометрит, возникающий вследствие инфекций, передающихся половым путем, большого числа инвазивных гинекологических вмешательств, эндометриоза матки (аденомиоз).
Диагностировать ановуляторный менструальный цикл довольно просто. Клинически для него характерна олигоменорея, то есть пациентка пожалуется на «нерегулярный менструальный цикл с задержками». Проведение УЗ исследования в зависимости от фазы цикла может подтвердить диагноз. В целом при УЗ исследовании на фоне ановуляции в яичниках можно обнаружить мелкие фолликулы (дисфункиональное маточное кровотечение вследствие атрезии фолликулов), персистирующий фолликул (дисфункциональное маточное кровотечение вследствие персистенции фолликулов). Толщина эндометрия будет зависеть от времени, прошедшего после последней менструации и количества эстрогенов, продуцируемых яичниками. Также важным критерием будет отсутствие желтого тела.
Для дисфункциональных маточных кровотечений, причиной которых является недостаточность желтого тела (НЛФ), характерна полименорея, то есть менструации у такой пациентки будут приходить регулярно, но менее, чем через 21 день. Диагностическими критериями для этого состояния могут быть: низкий уровень прогестерона во второй фазе менструального цикла при установленном факте овуляции, короткая (менее 10 дней) гипертермическая фаза на графике базальной температуры.
Лечение
Кровотечения в первой фазе менструального цикла чаще всего связаны с недостатком эстрогенов, который можно восполнить их введением извне, к примеру, в виде оральных контрацептивов.
К наиболее часто выявляемым органическим причинам маточных кровотечений относятся полипы эндометрия и цервикального канала, гиперпластический процесс эндометрия и кровотечения, обусловленные наличием миомы матки или внутреннего эндометриоза (аденомиоза). Все эти состояния с большой вероятностью можно выявить при УЗ исследовании в сочетании со стандартным клиническим обследованием.
Если механизм развития маточных кровотечений на фоне полипов и гиперплазии эндометрия очевиден, то в отношении причин маточных кровотечений, вызванных миомой матки, до сих пор нет однозначных мнений.
Таблица№1 Нормальные показатели менструального цикла
Что такое эндометрий в гинекологии?
Эндометрий – это особый слой, который выстилает внутреннюю поверхность матки. Его разделяют на функциональный (который отторгается при менструации) и базальный (который восстанавливается после месячных). Основная задача эндометрия матки – это создание наиболее благоприятных условий для имплантации эмбриона внутри матки.
Если его структура утолщается или становится более тонкой, то возникает реальная опасность того, что женщина не сможет выносить плод. Любые патологические процессы внутреннего слоя матки должны устраняться врачами на основании проведенных диагностических исследований.
ФУНКЦИИ ЭНДОМЕТРИЯ
Норма показателей толщины эндометрия матки при регулярном цикле продолжительностью 28 дней
| День цикла | Стадия | Толщина (м)м | Структура эндометрия | Количество слоёв |
| 1 – 2 | Фаза десквамации кровотечения | 5 – 9 | Неоднородная, с пониженной эхогенностью и повышенной звукопроводимостью | Отсутствуют |
| 3 – 4 | Фаза регенерации при кровотечении | 3 – 5 | С повышенной эхогенностью | Отсутствуют |
| 5 – 7 | Фаза ранней пролиферации | 6 – 9 | Эхогенность снижается при повышении звукопроводимости | Появление эхонегативного ободка (около 1 мм) |
| 8 – 10 | Фаза средней пролиферации | 8 – 10 | Появление чёткого гиперэхогенного образования размером в 1 мм и анэхогенного ободка (около 3 мм) | 3 |
| 11 – 14 | Фаза поздней пролиферации | 9 – 13 | Появление над ободком тонкой полоски размером около 1 мм. Создание благоприятных условий для оплодотворения | 4 |
| 15 – 18 | Фаза ранней секреции | 10 – 16 | Структура продолжает разделяться | 4 |
| 19 – 23 | Фаза средней секреции | 10 – 22 | Слизистая практически прекращает разрастаться, организм готовится отторгнуть её (если оплодотворения не произошло) | 4 |
| 24 – 27 | Фаза поздней секреции | 10,1 – 18 | Слизистая практически прекращает разрастаться, организм готовится отторгнуть её (если оплодотворения не произошло) | 4 |
Существуют различные патологии эндометрия матки. При этом возникать они могут в разном возрасте – им подвержены женщины репродуктивного возраста и находящиеся в периоде менопаузы.
ГИПОПЛАЗИЯ
Гипоплазия эндометрия матки – это патологическое состояние, при котором толщина слизистого слоя становится меньше. Это состояние негативно влияет на закрепление яйцеклетки после оплодотворения. Такая патология возникает из-за следующих причин:
Такое состояние может быть достаточно опасным. Здесь можно отметить не только проблемы с нормальным течением беременности, но и риск полного бесплодия женщины. Поэтому крайне важно выявлять патологию на ранних стадиях.
Проблема в том, что на этом этапе отсутствуют яркие симптомы, которые бы могли беспокоить пациентку. Выход один – проходить регулярные обследования у гинеколога, который может вовремя заметить истончение слизистого слоя матки в ходе УЗИ органов малого таза.
СИМПТОМЫ ГИПОПЛАЗИИ
При гипоплазии эндометрия матки у женщин могут встречаться следующие симптомы:
Вся эта симптоматика может быть причиной для обращения к врачу, но не должна использоваться для постановки 100% диагноза. Важно провести полное обследование, чтобы понять точную причину этих проявлений.
ГИПЕРПЛАЗИЯ
Под гиперплазией понимается утолщение эндометрия матки, при котором происходит изменение соотношения железистой ткани и стромы. Есть 2 типа этого патологического состояния:
В период менструации происходит обновление эндометрия и изменение гормонального фона. Все это сопровождается изменением концентрации эстрогена и прогестерона. Действие эстрогена приводит к утолщению слоя, а изменение уровня прогестерона приводит к разрушению эндометрия матки, если яйцеклетка не оплодотворена. Если все эти процессы протекают в нормальном режиме, то и менструальный цикл протекает без сбоев.
Появление гиперплазии обусловлено следующими факторами:
СИМПТОМЫ ГИПЕРПЛАЗИИ
У многих женщин изменения в слизистой оболочке матки протекают бессимптомно. Но если эндометрий увеличен, то это может привести к нарушению менструального цикла, которое характеризуется болями и достаточно сильным маточным кровотечением.
К дополнительной симптоматике относится:
Наши опытные врачи акушеры-гинекологи, УЗИ-специалисты и урологи
КАКИЕ ЕЩЕ ЕСТЬ ЗАБОЛЕВАНИЯ ЭНДОМЕТРИЯ?
В современной медицине есть различные заболевания эндометрия, каждые из которых имеют свои определенные причины возникновения, симптоматику и способы терапии. Вот основные из них:
КАК ДИАГНОСТИРУЮТСЯ ПАТОЛОГИИ ЭНДОМЕТРИИ?
При появлении у женщины симптоматики, характерной при поражениях эндометрии матки, нужно немедленно обратиться к врачу. Для начала пациентку направляют на стандартные лабораторные исследования – анализ мочи и крови. Проводится гинекологический осмотр, в ходе которого врач определяет изменения формы матки, проверяет толщину эндометрия – увеличен или истончен этот слой.
Есть и другие методы диагностики:
ИЗМЕНЕНИЕ ТОЛЩИНЫ ЭНДОМЕТРИЯ У ЖЕНЩИН В ПЕРИОД МЕНОПАУЗЫ
У женщины в период менопаузы должна быть определенная толщина эндометрия. Если она увеличивается, то есть риск развития ряда заболеваний. Для этого периода нормально, если в ходе УЗИ диагностируется сильное истончение слизистого слоя. Допустимая норма – не более 5 мм. Если толщина увеличивается до 6-7 мм, то за пациенткой должен осуществляться постоянный контроль, чтобы определить динамику этих изменений.
Изменения гормонального фона в период климакса – это абсолютно нормальное явление. Они влияют на работу множества внутренних органов, включая матку. Одним из наиболее часто встречающихся заболеваний является именно гиперплазия эндометрия. В этом возрасте она может проявляться следующей симптоматикой:
ПРИЧИНЫ ИЗМЕНЕНИЯ ТОЛЩИНЫ ЭНДОМЕТРИЯ В ПЕРИОД МЕНОПАУЗЫ
Чем старше становится женщина, тем больше изменений происходит в ее организме. С возрастом выработка эстрогена постепенно снижается, что сказывается на структуре эндометрия, который начинает атрофироваться. Истончается не только слизистый слой, но и уменьшается в размерах сама матка.
В климактерический период достаточно часто происходят гормональные сбои, которые приводят к тому, что слой продолжает увеличивать в размерах. Опасность этой ситуации в том, что своевременного отторжения эпителия не происходит (как при нормальном менструальном цикле). На утолщение слизистого слоя матки косвенно влияет:
СПОСОБЫ ЛЕЧЕНИЯ
Лечение различных патологий, происходящих в эндометрии матки, проводится двумя способами – консервативным или хирургическим. Такие кардинальные меры, как операция, проводятся в крайних случаях, когда медикаментозное лечение не дает нужного результата, либо оно изначально неэффективно.
Консервативное лечение женщин с заболеваниями эндометрия матки основывается на нескольких факторах. Важен возраст пациентки, фактическая стадия заболевания и то, планирует ли она в дальнейшем иметь детей.
Один из способов лечения – заместительная гормонотерапия. Здесь важно, чтобы прием этих средств был под контролем лечащего врача. Препараты для наращивания эпителия матки: «Дивигель», «Прогинова», «Дюфастон» и т.д.
Хирургическое лечение назначается в следующих случаях:
Изменение толщины и структуры эндометрия в матке – это потенциально опасное состояние, которое влияет на нормальное течение беременности. Возможны ситуации, при которых женщина и вовсе не может выносить ребенка.
Это состояние опасно и для пациенток не репродуктивного возраста, поэтому при появлении первой симптоматики нужно обратиться к врачу. Универсальный совет – это плановые посещения гинекологического кабинета, особенно если вы планируете беременность.
Если у Вас есть вопросы или нужна консультация врача гинеколога, оставьте свои контакты в одной из форм сайта или напишите в онлайн-чат.
Отзывы пациентов о наших врачах
Доктор очень хороший и внимательный. Он локализовал проблему и предложил нам пути решения. Мы благодарны этому врачу!
Доктор компетентный. Он собрал анамнез, провел осмотр, сделал УЗИ, ответил на вопросы и назначил анализы.
(Отзыв со СберЗдоровье. Оценка 5)
У доктора хороший психологический подход к пациентам и отношение. На приеме он меня осмотрел, пересмотрел УЗИ, сказал, что с почками, все хорошо, все объяснил и назначил лечение. Люди которые были в очереди в поликлинике, спрашивали именно об этом враче.
Доктор очень внимательный и чуткий. Анна Игоревна сделала мне УЗИ, все показала и рассказала.
Хронический эндометрит — проблема и решения
Рассмотрены факторы риска развития хронического эндометрита, клинические симптомы заболевания, методы диагностики и подходы к комплексной терапии.
An examination was performed on the factors of the risk of the development of chronic endometritis, clinical symptoms of disease, methods of diagnostics and approaches to complex therapy.
.jpg)
В настоящее время актуальность проблемы ХЭ приобретает не только медицинское, но и социальное значение, поскольку данное заболевание часто приводит к нарушению репродуктивной функции, являясь причиной бесплодия, неудачных попыток экстракорпорального оплодотворения (ЭКО), невынашивания беременности (НБ), осложненного течения беременности и родов [1].
Хронический эндометрит — клинико-морфологический синдром, характеризующийся комплексом морфофункциональных изменений эндометрия воспалительного генеза, приводящих к нарушению нормальной циклической трансформации и рецептивности ткани.
Среди пациенток с ХЭ 97,6% составляют женщины репродуктивного периода, что подчеркивает особую значимость данной патологии с точки зрения влияния на репродуктивную функцию [2].
У женщин с бесплодием ХЭ встречается в 12–68% случаев, достигая своего максимума при наличии трубно-перитонеального фактора бесплодия. У больных с неудачными попытками ЭКО и переноса эмбрионов (ПЭ) частота ХЭ возрастает до 60% и более. Наибольшие показатели распространенности ХЭ отмечены у больных с привычным невынашиванием беременности и составляют более 70% [5, 6].
По данным различных авторов, факторами риска развития ХЭ являются все инвазивные вмешательства в полости матки (гистероскопия, выскабливание полости матки, биопсия эндометрия, гистеросальпингография, манипуляции в программах вспомогательных репродуктивных технологий и др.), инфекционно-воспалительные осложнения после беременностей и родов, использование внутриматочных спиралей (ВМС), инфекции влагалища и шейки матки, бактериальный вагиноз, деформации полости матки с нарушением циклического отторжения эндометрия, лучевая терапия в области органов малого таза [1, 7, 8].
В современных условиях эндометрит характеризуется рядом особенностей: изменением этиологической структуры с увеличением значимости вирусной и условно-патогенной флоры, ростом резистентности флоры к фармакотерапии, трансформацией клинической симптоматики в сторону стертых форм и атипичного течения, длительными сроками терапии и высокой ее стоимостью [9]. Современная общепризнанная классификация ХЭ, выстроенная по этиологическому фактору, претерпела в последнее десятилетие значительные изменения в сторону расширения перечня специфических форм заболевания. Существуют вирусные (вирус папилломы человека — ВПЧ, цитомегаловирус, вирус иммунодефицита человека), хламидийные, микоплазменные, грибковые, протозойные и паразитарные специфические эндометриты, отдельно выделен саркоидоз эндометрия [1, 10]. Для идентификации инфекционного агента обязательно проводить тщательное микробиологическое исследование соскоба эндометрия с определением чувствительности флоры к антибактериальным препаратам. В одной трети случаев при гистологически верифицированном ХЭ выявляются стерильные посевы эндометрия, что может свидетельствовать о важной роли условно-патогенной флоры в развитии воспалительного процесса или недостаточной детекции возбудителя, особенно в случае вирусной инвазии [11]. Длительная и часто бессимптомная персистенция инфекционных агентов в эндометрии приводит к выраженным изменениям в структуре ткани, препятствуя нормальной имплантации и плацентации, формируя патологический ответ на беременность, а также вызывает нарушение пролиферации и нормальной циклической трансформации ткани [12]. По различным данным, у больных с бесплодием частота ХЭ составляет в среднем 10% (от 7,8 до 15,4%). Среди женщин с верифицированным ХЭ в 60% случаев диагностируется бесплодие (в 22,1% — первичное бесплодие, в 36,5% — вторичное бесплодие), неудачные попытки ЭКО и переноса эмбрионов в анамнезе отмечены у 40% женщин [4, 12]. Клиническая картина ХЭ в значительной степени отражает глубину структурных и функциональных изменений в ткани эндометрия. Неполноценная циклическая трансформация эндометрия на фоне воспалительного процесса, нарушение процессов десквамации и регенерации функционального слоя эндометрия приводят к появлению основного симптома заболевания — маточных кровотечений (перименструальные, межменструальные). Достаточно постоянными являются жалобы на тянущие боли внизу живота, дисменорею и диспареунию, нередко отмечаются серозные и серозно-гноевидные бели. Среди клинических симптомов особое место занимает бесплодие (преимущественно вторичное), неудачные попытки ЭКО и НБ. Более половины пациенток в анамнезе имеют инвазивные вмешательства в полости матки и на органах малого таза. Часто хронический эндометрит сочетается с хроническим сальпингоофоритом и спаечным процессом в малом тазе. Важно отметить, что использование минимальных критериев для диагностики воспалительных заболеваний органов малого таза (ВЗОМТ), предложенных CDC (Centers for Disease Control and Prevention, США, 1993), информативно в случае с хроническим эндометритом только в 33% [7]. В целом у 35–40% пациенток какие-либо клинические симптомы заболевания отсутствуют [8, 13]. Диагностика ХЭ основана на анализе клинических симптомов, данных анамнеза, эхографической картины [2, 11]. Обязательным этапом диагностики заболевания является морфологическое исследование эндометрия [14].
Эхографические критерии ХЭ впервые разработаны профессором В. Н. Демидовым с соавт. (1993 г.). Исследование проводят дважды на 5–7 и 17–21 день менструального цикла. Часто при ХЭ полость матки после менструации расширена до 0,4–0,7 см, в ряде случаев имеется асимметричность расширения полости матки и неровность внутренней поверхности эндометрия. Изменение структуры эндометрия также выражается в возникновении в зоне срединного М-эха участков повышенной эхогенности различной величины и формы. Внутри участков выявляются отдельные зоны неправильной формы и сниженной эхогенности. Другой важный признак — наличие пузырьков газа, иногда с характерным акустическим эффектом «хвоста кометы». В базальном слое эндометрия часто визуализируются четкие гиперэхогенные образования диаметром до 0,1–0,2 см, представляющие собой очаги фиброза, склероза или кальциноза. Довольно редким, но важным признаком эндометрита является асимметрия толщины передней и задней стенок эндометрия. О наличии патологии свидетельствует также истончение М-эха во второй трети менструального цикла менее 0,6 см. У каждой пятой больной отмечается наличие нескольких из перечисленных признаков [15].
В настоящее время для диагностики внутриматочной патологии широко используется гистероскопия [16]. Наиболее частыми признаками воспалительного процесса в эндометрии являются: неравномерная толщина эндометрия — 30% случаев, полиповидные нарастания — 32,2%, неравномерная окраска и гиперемия слизистой оболочки — 23% и 11,8%, точечные кровоизлияния — 9%, очаговая гипертрофия слизистой оболочки — 7%. Трудности гистероскопической интерпретации данных связаны с отсутствием типичных макроскопических признаков хронического эндометрита, с очаговым характером воспалительного процесса и стертыми формами заболевания [17]. По разным данным гистероскопия позволяет по макроскопическим признакам точно идентифицировать хронический эндометрит только в 16–35% случаев [7, 16]. При подозрении на ХЭ гистероскопия важна для исключения всего спектра внутриматочной патологии, но для верификации диагноза во всех случаях необходимо проведение морфологического исследования эндометрия [8].
«Золотым стандартом» диагностики ХЭ является морфологическое исследование эндометрия, которое должно быть обязательным звеном алгоритма обследования [7, 13]. Диагностическое выскабливание слизистой оболочки матки производят в среднюю и позднюю фазу пролиферации, на 7–10 день менструального цикла. В последние годы общепринятыми критериями морфологической диагностики ХЭ являются [1]:
Несмотря на значительное развитие фармакологической основы терапии, лечение ХЭ в настоящее время представляет значительные трудности для клиницистов [4].
Комплексная терапия ХЭ должна быть этиологически и патогенетически обоснованной, поэтапной и базироваться на результатах максимально тщательного обследования [5]. Алгоритм лечения должен учитывать все звенья патогенеза заболевания.
Необходимость использования этиотропных препаратов для элиминирования повреждающего агента или снижение вирусной активности не вызывает сомнения. Принимая во внимание, что почти в 70% случаев ВЗОМТ применение рутинных методов диагностики не позволяет выявить этиологический фактор, эмпирическая антимикробная терапия при ХЭ всегда оправдана и приводит к достоверному уменьшению частоты клинических симптомов. При этом она должна обеспечивать элиминацию широкого спектра возможных патогенных микроорганизмов, включая хламидии, гонококки, трихомонады, грамотрицательные факультативные бактерии, анаэробы, стрептококки и вирусы. Оправдано назначение нескольких курсов этиотропной терапии со сменой групп препаратов [5, 18].
Выбор группы лекарственных препаратов зависит от данных микробиологического исследования содержимого влагалища и полости матки, анамнестических указаний на использование антибактериальных препаратов в течение последнего года, от выраженности клинической симптоматики и обширности воспалительного процесса [16].
Основу базовой антибактериальной терапии должны составлять комбинации фторхинолонов и нитроимидазолов; цефалоспоринов III поколения, макролидов и нитроимидазолов, а также сочетание защищенных пенициллинов (амоксициллин/клавулановая кислота) с макролидами. При наличии вирусной инфекции (чаще вируса простого герпеса) в зависимости от клинической картины применяют современные аналоги нуклеозидов (Ацикловир или Валтрекс), как правило, в длительном режиме — в течение не менее 3–4 месяцев [3, 19].
Одновременно на основании данных иммунного и интерферонового статуса проводится коррекция иммунных нарушений [20].
Второй этап лечения ХЭ направлен на восстановление морфофункционального потенциала ткани и устранение последствий вторичных повреждений: коррекция метаболических нарушений и последствий ишемии, восстановление гемодинамики и активности рецепторного аппарата эндометрия. Данный этап лечения крайне важен, должен быть продуманным и достаточно продолжительным [11].
Метаболическая терапия при ХЭ направлена на усиление тканевого обмена, активацию энергетических процессов в клетках, устранение последствий гипоксии ткани, в том числе угнетение анаэробного гликолиза [4, 12]. С этой целью используются комплексные метаболические препараты, длительность приема которых должна составлять не менее 3–4 недель. Представителем данной группы препаратов является Актовегин, полученный посредством диализа и ультрафильтрации, в состав которого входят низкомолекулярные пептиды и дериваты нуклеиновых кислот. Актовегин активирует клеточный метаболизм путем увеличения транспорта, накопления и усиления внутриклеточной утилизации глюкозы и кислорода, что приводит к ускорению метаболизма аденозинтрифосфата (АТФ) и повышению энергетических ресурсов клетки. Актовегин удобен для приема. Его выпускают и в таблетках, и в растворе для инъекций. Поэтому женщины, которые по каким-либо причинам не могут лечь в стационар или систематически приезжать на прием, принимают его дома по схеме, расписанной врачом. Актовегин таблетки принимают, не разжевывая, перед едой, запивая небольшим количеством жидкости, по 1 таблетке 2 раза в день в течение 30 дней [21]. При введении в форме инфузии к 200–300 мл основного раствора (0,9% раствор хлорида натрия или 5% раствор декстрозы) добавляют 10–20 мл Актовегина, раствор используют по следующей схеме: внутривенно через день в течение не менее двух недель. Скорость введения: около 2 мл/мин [22].
Положительное влияние Актовегина на кровообращение связано с улучшением доставки и утилизации кислорода, увеличением перфузии глюкозы и восстановлением аэробного метаболизма как в периферических тканях, так и в нейрональных структурах. Путем активации фермента супероксиддисмутазы препарат оказывает выраженное антиоксидантное и противоишемическое действие. Актовегин хорошо сочетается с другими лекарственными средствами, что очень удобно для комплексного лечения хронического эндометрита.
Традиционно в комплексной терапии ХЭ применяются физические факторы. Наиболее часто в комплексной терапии ХЭ применяют электроимпульсную терапию, интерференционные токи, переменное магнитное поле низкой частоты, ток надтональной частоты. Задачи физиотерапии при ХЭ заключаются в улучшении гемодинамики органов малого таза, стимуляции функции рецепторов, ускорении процессов регенерации эндометрия, повышении иммунологических свойств [4].
Дискуссионными остаются вопросы о целесообразности использования в комплексном лечении ХЭ циклической гормональной терапии. В настоящее время считается, что при хроническом эндометрите оправдано только дифференцированное назначение гормонотерапии при наличии гипофункции яичников или ановуляции. Потенциал к патологической регенерации ткани, который таит в себе хроническое воспаление, при назначении циклической заместительной гормональной терапии может быть усилен и реализован [3, 8].
Контроль эффективности терапевтических мероприятий должен проводиться не ранее чем через 2 месяца после окончания лечения с учетом эффекта последействия физиотерапии [2, 5]. При этом оценивается динамика клинических симптомов, проводится ультразвуковое исследование матки (допплерометрия сосудов матки) и аспирационная биопсия эндометрия (на 7–10 день менструального цикла) с последующим морфологическим исследованием эндометрия [1, 11].
Литература
А. З. Хашукоева, доктор медицинских наук, профессор
Н. Д. Водяник, кандидат медицинских наук, доцент
С. А. Хлынова, кандидат медицинских наук
Е. А. Цомаева
ГБОУ ВПО РНИМУ им. Н. И. Пирогова Минздравсоцразвития России, Москва