Аэробная и анаэробная среда
При выполнении гематологических исследований используются два типа организмов аэробные и анаэробные. Они отличаются потребностью в наличии кислорода в окружающей среде. Аэробные микроорганизмы могут функционировать только при наличии кислорода, в то время, как анаэробные в нем совсем не нуждаются.
Классификация этих видов проводится на основе реакции на наличие или отсутствие кислорода. Из-за этого аэробные и анаэробные микроорганизмы по-разному выполняют свои функции в процессе клеточного дыхания.
Особенности аэробных микроорганизмов
Аэробные микроорганизмы не могут существовать без кислорода. Он необходим им для роста, развития и участвует в процессах размножения. Благодаря кислороду они способны окислять моносахариды, например, глюкозу.
Генерация энергии в этих микроорганизмах происходит при гликолизе. После него следует цикл Кребса и цепь переноса электронов. Среды, насыщенные кислородом – отличная питательная среда для таких микроорганизмов. Примеры аэробов – бациллы и нокардии.
Типы аэробов
Аэробные микроорганизмы классифицируют по уровню необходимого для жизнедеятельности кислорода:
Бактерии, нуждающиеся в кислороде для выживания, легко выделяются при культивировании в жидкой среде. Так для полноценной жизнедеятельности им необходим кислород, то чтобы выжить они всплывают на поверхность.
Особенности анаэробов
В процессе энергетического обмена эти микроорганизмы не используют кислород. Для этого им необходимы марганец, сера, кобальт, азот, метал или железо. В процессе образования энергии анаэробные микроорганизмы подвергаются ферментации. Для выживания они используют энергию, производимую при анаэробных процессах брожения:
Классификация анаэробных микроорганизмов также определяется по уровню токсичности кислорода:
Анаэробы не способны выживать в среде, богатой кислородом. Для облигатных разновидностей он токсичен, а вот факультативным видам он не вредит.
Сходства между аэробами и анаэробами
Различия аэробов и анаэробов
Отличительные особенности микроорганизмов представлены в таблице.
Анаэробная инфекция
Анаэробная инфекция – это инфекционный процесс, вызываемый спорообразующими или неспорообразующими микроорганизмами в условиях, благоприятных для их жизнедеятельности. Характерными клиническими признаками анаэробной инфекции служат преобладание симптомов эндогенной интоксикации над местными проявлениями, гнилостный характер экссудата, газообразующие процессы в ране, быстро прогрессирующий некроз тканей. Анаэробная инфекция распознается на основании клинической картины, подтвержденной результатами микробиологической диагностики, газожидкостной хроматографии, масс-спектрометрии, иммуноэлектрофореза, ПЦР, ИФА и др. Лечение анаэробной инфекции предполагает радикальную хирургическую обработку гнойного очага, интенсивную дезинтоксикационную и антибактериальную терапию.
МКБ-10
Общие сведения
Анаэробная инфекция – патологический процесс, возбудителями которого выступают анаэробные бактерии, развивающиеся в условиях аноксии (отсутствия кислорода) или гипоксии (низкого напряжения кислорода). Анаэробная инфекция представляет собой тяжелую форму инфекционного процесса, сопровождающуюся поражением жизненно важных органов и высоким процентом летальности. В клинической практике с анаэробной инфекцией приходится сталкиваться специалистам в области хирургии, травматологии, педиатрии, нейрохиругии, отоларингологии, стоматологии, пульмонологии, гинекологии и других медицинских направлений. Анаэробная инфекция может возникнуть у пациентов любого возраста. Доля заболеваний, вызываемых анаэробной инфекцией, точно не известна; из гнойных очагов в мягких тканях, костях или суставах анаэробы высеваются примерно в 30% случаев; анаэробная бактериемия подтверждается в 2-5% случаев.
Причины
Анаэробы входят в состав нормальной микрофлоры кожи, слизистых оболочек, желудочно-кишечного тракта, органов мочеполовой системы и по своим вирулентным свойствам являются условно-патогенными. При определенных условиях они становятся возбудителями эндогенной анаэробной инфекции. Экзогенные анаэробы присутствуют в почве и разлагающихся органических массах и вызывают патологический процесс при попадании в рану извне. Анаэробные микроорганизмы делятся на:
Факторы риска
Условиями, благоприятствующими развитию анаэробной инфекции, являются повреждение анатомических барьеров с проникновением анаэробов в ткани и кровеносное русло, а также снижение окислительно-восстановительного потенциала тканей (ишемия, кровотечение, некроз). Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.), перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах и т. д. Факторами, способствующими возникновению анаэробной инфекции, выступают:
Кроме этого, большое значение имеет нерациональная антибиотикотерапия, направленная на подавление сопутствующей аэробной микрофлоры.
Патогенез
Основными факторами патогенности анаэробных микроорганизмов служат их количество в патологическом очаге, биологические свойства возбудителей, наличие бактерий-ассоциантов. В патогенезе анаэробной инфекции ведущая роль принадлежит продуцируемым микроорганизмами ферментам, эндо- и экзотоксинам, неспецифическим факторам метаболизма. Так, ферменты (гепариназа, гиалуронидаза, коллагеназа, дезоксирибонуклеаза) способны усиливать вирулентность анаэробов, деструкцию мышечной и соединительной тканей.
Классификация
В зависимости от локализации различают анаэробную инфекцию:
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток).
Симптомы анаэробной инфекции
Независимо от вида возбудителя и локализации инфекционного очага, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Типичным признаком анаэробной инфекции служит преобладание симптомов общей интоксикации над местными воспалительными явлениями. Резкое ухудшение общего состояния больного обычно наступает еще до возникновения локальных симптомов. Проявлением тяжелого эндотоксикоза служит высокая лихорадка с ознобами, выраженная слабость, тошнота, головная боль, заторможенность. Характерны артериальная гипотония, тахипноэ, тахикардия, гемолитическая анемия, иктеричность кожи и склер, акроцианоз.
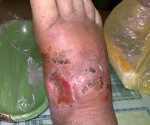
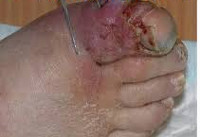
При раневой анаэробной инфекции ранним местным симптомом выступает сильная, нарастающая боль распирающего характера, эмфизема и крепитация мягких тканей, обусловленные газообразующими процессами в ране. К числу постоянных признаков относится зловонный ихорозный запах экссудата, связанный с выделением азота, водорода и метана при анаэробном окислении белкового субстрата. Экссудат имеет жидкую консистенцию, серозно-геморрагический, гнойно-геморрагический или гнойный характер, неоднородную окраску с вкраплениями жира и наличием пузырьков газа. На гнилостный характер воспаления также указывает внешний вид раны, содержащей ткани серо-зеленого или серо-коричневого цвета, иногда струпы черного цвета.
Осложнения
Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Диагностика
Для своевременной диагностики анаэробной инфекции большое значение имеет правильная оценка клинических симптомов, позволяющая своевременно оказать необходимую медицинскую помощь. В зависимости от локализации инфекционного очага диагностикой и лечением анаэробной инфекции могут заниматься клиницисты различных специальностей – общие хирурги, травматологи, нейрохирурги, гинекологи, отоларингологи, челюстно-лицевые и торакальные хирурги. С целью определения патогенного агента и тяжести инфекционного процесса используют:
Анаэробную инфекцию необходимо дифференцировать от рожистого воспаления мягких тканей, полиморфной экссудативной эритемы, тромбоза глубоких вен, пневмоторакса, пневмоперитонеума, перфорации полых органов брюшной полости.
Лечение анаэробной инфекции
Комплексный подход к лечению анаэробной инфекции предполагает проведение радикальной хирургической обработки гнойного очага, интенсивной дезинтоксикационной и антибактериальной терапии. Хирургический этап должен быть выполнен как можно раньше – от этого зависит жизнь больного. Как правило, он заключается в широком рассечении очага поражения с удалением некротизированных тканей, декомпрессии окружающих тканей, открытом дренировании с промыванием полостей и ран растворами антисептиков. Особенности течения анаэробной инфекции нередко требуют проведения повторных некрэктомий, раскрытия гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т. д. При обширной деструкции тканей может быть показана ампутация или экзартикуляция конечности.
Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, высокотропными к анаэробам. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, УФОК, экстракорпоральная гемокоррекция (гемосорбция, плазмаферез и др.). При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
Прогноз и профилактика
Исход анаэробной инфекции во многом зависит от клинической формы патологического процесса, преморбидного фона, своевременности установления диагноза и начала лечения. Уровень летальности при некоторых формах анаэробной инфекции превышает 20%. Профилактика анаэробной инфекции заключается в своевременной и адекватной ПХО ран, удалении инородных тел мягких тканей, соблюдении требований асептики и антисептики при проведении операций. При обширных раневых повреждениях и высоком риске развития анаэробной инфекции необходимо проведение специфической иммунизации и противомикробной профилактики.
Anaerovibrio (анаэробные бактерии)
Анаэробные бактерии (Anaerovibrio) живут в организме человека в желудочно-кишечном тракте. Обитают также в толстой кишке и приносят большую пользу для организма.
Для своей жизнедеятельности этот тип бактерий не нуждается в кислороде. Поэтому живут и размножаются внутри ЖКТ. Кроме организма человека, анаэробные бактерии обитают также в рубце овец и крупного рогатого скота.
Бактерии этого вида необходимы для нормального функционирования организма человека и животных. При недостаточном содержании этих бактерий, нарушается работа различных органов.
Поэтому они привлекают пристальное внимание ученых. Анаэробные бактерии продолжают изучать с помощью современного оборудования. Это открывает из новые свойства и качества.
Какие основные свойства анаэробных бактерий?
В процессе жизнедеятельности анаэробные бактерии производят необходимые для нормальной деятельности организма человека и животных короткоцепочечные жирные кислоты. Кроме этого, они обеспечивают организм необходимым количеством уксусной и пропионовой кислоты.
Анаэробные бактерии входят в обширную группу микроорганизмов, которые играют важную роль в жизнедеятельностиорганизма. Впервые этот термин ввел ученый Луи Пастер, который открыл анаэробы в 1861 году, в процессе маслянокислого брожения. С момента своего открытия анаэробы продолжат изучать.
К какому роду бактерий относятся анаэробы?
Семейство и род анаэробных бактерий меняло свое название. Сначала род анаэробных бактерий относили к семейству Acidaminococcaceae. С развитием науки и знаний о свойствах анаэробных бактерий, это семейство упразднили.
Используя современную классификацию, бактерии этого рода входят в семейство Selenomonadaceae, царство Бактерий. Группа без ранга. В настоящее время к роду анаэробных бактерий ученые относят только один вид под названием Anaerovibrio lipolyticus.
В ранней классификации в род бактерий входил еще один вид. Но современные ученые произвели реклассификацию. В результате бактерии рода Anaerovibrio переименовали в род Anaerosinus.
Свое второе название получили также бактерии вида Anaerovibrio burkinabensis. После дополнительного изучения свойств и особенностей, ученые переименовали этот вид бактерий в род под названием Anaeroarcus.
Эти полезные для жизнедеятельности организма человека бактерии продолжают изучать. Новые методы и технологии позволяют обнаруживать неизвестные ранее свойства.
Факультативно анаэробные микроорганизмы что это такое
Микробиологическое исследование на анализаторе VITEK bioMerieux, позволяющее с более высокой чувствительностью и специфичностью, чем обычный посев, идентифицировать около 200 видов клинически значимых бактерий и подобрать антибиотикотерапию с расчетом минимальной эффективной дозировки препарата. Преимущества исследования по сравнению с обычным посевом: срок выполнения короче на 24 часа; чувствительность определяется к расширенному списку антибиотиков (до 20 шт.); результат выдается как в виде критических значений (чувствителен, умеренно-устойчив, устойчив), так и в виде значений минимальных ингибирующих концентраций антибиотика (МИК). Что, в свою очередь, позволяет выбрать наиболее эффективную минимальную дозу антибиотика, снизив его негативное влияние на человеческий организм. * Чувствительность к антибиотикам будет определена при выявлении патогенных и/или условно-патогенных микроорганизмов. При обнаружении микроорганизмов, составляющих нормальную микрофлору, чувствительность к антибиотикам не определяется, т.к. не имеет диагностического значения.
Бактериологическое исследование клинического материала с определением чувствительности к антибиотикам на анализаторе VITEK bioMerieux; посев на микрофлору в аэробных условиях.
Какой биоматериал можно использовать для исследования?
Грудное молоко, мазок из десневого кармана, мазок из зева, мазок с конъюнктивы, мазок из носа, мазок из носоглотки, мазок урогенитальный (с секретом предстательной железы), мокроту, отделяемое уха, рвотные массы, синовиальную жидкость, смыв из бронхов, соскоб с кожи, среднюю порцию утренней мочи, эякулят.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Анаэробная микрофлора – это микроорганизмы, для жизнедеятельности и размножения которых не требуется кислород, для многих из них он, наоборот, является губительным. Анаэробы населяют организм человека в норме (в пищеварительном тракте, органах дыхания, мочеполовой системе). При снижении иммунитета или травмах, повреждениях возможна активация инфекции с развитием воспалительного процесса. Организм человека тогда может становиться по сути источником заражения сам для себя (эндогенное инфицирование). Реже анаэробы попадают в организм снаружи (глубокая колотая рана, инфицированный аборт, ранения брюшной и грудной полости, введение спиц и протезов). Развиваясь в толще кожи, мягких тканей и мышц, анаэробные организмы способны вызывать целлюлиты, абсцессы, миозиты. Симптомы, позволяющие заподозрить анаэробную инфекцию мягких тканей: плотный отёк, газообразование (ощущение, что лопаются пузырьки воздуха под кожей при надавливании), гнилостное воспаление, зловонный запах.
Основное лечение анаэробного воспаления – хирургическое. При этом необходимо устранить источник воспаления либо раскрыть рану, обеспечив доступ кислорода, губительного для анаэробов.
Жизнедеятельность аэробной флоры возможна лишь при наличии свободного кислорода. В отличие от анаэробов, у них он участвует в процессе выработки энергии, необходимой им для размножения. Эти бактерии не имеют выраженного ядра. Они размножаются почкованием или делением, при окислении образуя токсичные продукты. Культивирование аэробных бактерий подразумевает не только использование подходящей для них питательной среды, но также и количественный контроль кислородной атмосферы и поддерживание оптимальных температур. Для каждого микроорганизма данной группы существует минимум и максимум кислородной концентрации в среде, окружающей его, необходимой для его нормального размножения и развития.
Факультативные анаэробы – организмы, которые существуют и выполняют все энергетические и репродуктивные циклы по анаэробному пути, но при этом при этом способны существовать и развиваться в присутствии кислорода. Последней характеристикой облигатные и факультативные анаэробы и отличаются, т.к. облигатные не способны существовать в условиях кислорода и при его появлении гибнут. Всю необходимую для своего существования, развития и размножения энергию факультативные анаэробы получают с помощью расщепления органических и неорганических соединений.
Для дифференциальной диагностики анаэробной и аэробной инфекции проводят посев биоматериала на флору, так как принципы лечения в том или ином случае будут разные. По выросшей культуре определяется вид микроорганизмов, которые участвуют в формировании воспалительной реакции. Зная вид возбудителя, можно подобрать антибактериальный препарат, который способен успешно влиять на данные микроорганизмы.
В ходе данного исследования определяется наличие аэробной и факультативно-анаэробной флоры.
Микробиологическое исследование на анализаторе VITEK bioMerieux позволяет с более высокой чувствительностью и специфичностью, чем обычный посев, идентифицировать около 200 видов клинически значимых бактерий и подобрать антибиотикотерапию с расчетом минимальной эффективной дозировки препарата. Система анализатора предназначена для идентификации грамотрицательных палочек, грамположительных кокков, анаэробных бактерий, нейссерий, гемофильных палочек, других прихотливых бактерий, коринбактерий, лактобактерий, бацилл, грибов (более 450 таксонов). Система анализатора состоит из анализатора бактериологического и персонального компьютера. Автоматизация процесса снижает риск контаминации материала и ошибок в результатах исследования.
После выявления культуры бактерий целесообразно провести определение их чувствительности к разным антибиотикам. Зная вид возбудителя, можно подобрать антибактериальный препарат, который способен успешно влиять на данные микроорганизмы. В связи с тем что все чаще наблюдается развитие антибиотикорезистентности микроорганизмов, подбор антибиотиков по их спектру действия на бактерии может привести к малоэффективному или вообще безрезультатному лечению. Преимуществом метода определения чувствительности к антибиотикам является точное определение антибактериального препарата, имеющего наивысшую эффективность в конкретном случае.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Данное исследование не предусматривает выделение анаэробной микрофлоры, вирусов, хламидий, а также микроорганизмов, требующих особых условий культивирования, таких как Neisseria meningitidis, Neisseria gonorrhoeae, Bordetella pertussis, Bordetella parapertussis, Corynebacterium diphtheriae, Mycoplasma spp, Ureaplasma spp, Mycobacterium tuberculosis. При отсутствии роста диагностически значимой микрофлоры при бактериологическом посеве и наличии клинической картины рекомендуется назначение дополнительных исследований.
Кто назначает исследование?
Инфекционист, терапевт, гинеколог, врач общей практики, оториноларинголог, педиатр.
Кишечная микрофлора и значение пребиотиков для ее функционирования
Микрофлора кишечника человека является составляющей человеческого организма и выполняет многочисленные жизненно важные функции. Общая численность микроорганизмов, обитающих в различных частях макроорганизма, приблизительно на два порядка превышает числен
У здоровых лиц в кишечнике насчитывается более 500 видов микроорганизмов. Общая масса микрофлоры кишечника составляет от 1 до 3 кг. В разных отделах ЖКТ количество бактерий различно, большинство микроорганизмов локализованы в толстой кишке (около 10 10–12 КОЕ/мл, что составляет 35–50% ее содержимого). Состав кишечной микрофлоры достаточно индивидуален и формируется с первых дней жизни ребенка, приближаясь к показателям взрослого к концу 1-го — 2-му году жизни, претерпевая некоторые изменения в пожилом возрасте (табл. 1). У здоровых детей в толстой кишке обитают представители факультативно-анаэробных бактерий рода Streptococcus, taphylococcus, Lactobacillus, nterobacteriacae, Candida и более чем 80% биоценоза занимают анаэробные бактерии, чаще грамположительные: пропионобактерии, вейлонеллы, эубактерии, анаэробные лактобациллы, пептококки, пептострептококки, а также грамотрицательные бактероиды и фузобактерии.
Вся совокупность микроорганизмов и макроорганизм составляют своеобразный симбиоз, где каждый извлекает выгоды для своего существования и оказывает влияние на партнера. Функции кишечной микрофлоры по отношению к макроорганизму реализуются как локально, так и на системном уровне, при этом различные виды бактерий вносят свой вклад в это влияние. Микрофлора пищеварительного тракта выполняет следующие функции.
Так, бифидобактерии за счет ферментации олиго- и полисахаридов продуцируют молочную кислоту и ацетат, которые обеспечивают бактерицидную среду, секретируют вещества-ингибиторы роста патогенных бактерий, что повышает резистентность организма ребенка к кишечным инфекциям. Модуляции иммунного ответа ребенка бифидобактериями также выражаются в снижении риска развития пищевой аллергии.
Лактобациллы уменьшают активность пероксидазы, оказывая антиоксидантный эффект, обладают противоопухолевой активностью, стимулируют продукцию иммуноглобулина А (IgA), подавляют рост патогенной микрофлоры и стимулируют рост лакто- и бифидофлоры, оказывают противовирусное действие.
Из представителей энтеробактерий наиболее важное значение имеет Escherichia coli M17, которая вырабатывает колицин В, за счет чего подавляет рост шигелл, сальмонелл, клебсиелл, серраций, энтеробактеров и оказывает незначительное влияние на рост стафилококков и грибов. Также кишечная палочка способствуют нормализации микрофлоры после антибактериальной терапии и воспалительных и инфекционных заболеваний.
Кишечные палочки, бифидо- и лактобактерии выполняют витаминообразующую функцию (участвуют в синтезе и всасывании витаминов К, группы В, фолиевой и никотиновой кислот). По способности синтезировать витамины кишечная палочка превосходит все остальные бактерии кишечной микрофлоры, синтезируя тиамин, рибофлавин, никотиновую и пантотеновую кислоты, пиридоксин, биотин, фолиевую кислоту, цианокобаламин и витамин К. Бифидобактерии синтезируют аскорбиновую кислоту, бифидо- и лактобактерии способствуют всасыванию кальция, витамина D, улучшают всасывание железа (благодаря созданию кислой среды).
Процесс пищеварения условно можно разделить на собственное (дистанционное, полостное, аутолитическое и мембранное), осуществляемое ферментами организма, и симбиозное пищеварение, происходящее при содействии микрофлоры. Микрофлора кишечника человека участвует в ферментации нерасщепленных ранее компонентов пищи, главным образом углеводов, таких, как крахмал, олиго- и полисахариды (в том числе и целлюлоза), а также белков и жиров.
Не всосавшиеся в тонкой кишке белки и углеводы в слепой кишке подвергаются более глубокому бактериальному расщеплению — преимущественно кишечной палочкой и анаэробами. Конечные продукты, образующиеся в результате процесса бактериальной ферментации, оказывают различное влияние на состояние здоровья человека. Например, бутират необходим для нормального существования и функционирования колоноцитов, является важным регулятором их пролиферации и дифференцировки, а также всасывания воды, натрия, хлора, кальция и магния. Вместе с другими летучими жирными кислотами он оказывает влияние на моторику толстой кишки, в одних случаях ускоряя ее, в других — замедляя. При расщеплении полисахаридов и гликопротеинов внеклеточными микробными гликозидазами образуются, помимо прочего, моносахариды (глюкоза, галактоза и т. д.), при окислении которых в окружающую среду выделяется в виде тепла не менее 60% их свободной энергии.
Среди важнейших системных функций микрофлоры — поставка субстратов глюконеогенеза, липогенеза, а также участие в метаболизме белков и рециркуляции желчных кислот, стероидов и других макромолекул. Превращение холестерина в не всасывающийся в толстой кишке копростанол и трансформация билирубина в стеркобилин и уробилин возможны только при участии бактерий, находящихся в кишечнике.
Протективная роль сапрофитной флоры реализуется как на местном, так и на системном уровнях. Создавая кислую среду, благодаря образованию органических кислот и снижению рН среды толстой кишки до 5,3–5,8, симбионтная микрофлора защищает человека от колонизации экзогенными патогенными микроорганизмами и подавляет рост уже имеющихся в кишечнике патогенных, гнилостных и газообразующих микроорганизмов. Механизм этого явления заключается в конкуренции микрофлоры за питательные вещества и участки связывания, а также в выработке нормальной микрофлорой определенных ингибирующих рост патогенов субстанций, обладающих бактерицидной и бактериостатической активностью, в том числе антибиотикоподобных. Низкомолекулярные метаболиты сахаролитической микрофлоры, в первую очередь летучие жирные кислоты, лактат и др., обладают заметным бактериостатическим эффектом. Они способны ингибировать рост сальмонелл, дизентерийных шигелл, многих грибов.
Также кишечная микрофлора усиливает местный кишечный иммунологический барьер. Известно, что у стерильных животных в lamina propria определяется очень малое количество лимфоцитов, кроме того, у этих животных наблюдается иммунодефицит. Восстановление нормальной микрофлоры быстро приводит к увеличению количества лимфоцитов в слизистой кишечника и исчезновению иммунодефицита. Сапрофитные бактерии в определенной степени обладают способностью модулировать уровень фагоцитарной активности, снижая его у людей, страдающих аллергией и, наоборот, повышая его у здоровых индивидуумов.
Таким образом, микрофлора ЖКТ не только формирует местный иммунитет, но и играет огромную роль в становлении и развитии иммунной системы ребенка, а также поддерживает ее активность у взрослого. Резидентная флора, особенно некоторые микроорганизмы, обладают достаточно высокими иммуногенными свойствами, что стимулирует развитие лимфоидного аппарата кишечника и местный иммунитет (в первую очередь за счет усиления продукции ключевого звена системы местного иммунитета — секреторного IgA), а также приводит к системному повышению тонуса иммунной системы, с активацией клеточного и гуморального звеньев иммунитета. Системная стимуляция иммунитета — одна из важнейших функций микрофлоры. Известно, что у безмикробных лабораторных животных не только подавлен иммунитет, но и происходит инволюция иммунокомпетентных органов. Поэтому при нарушениях микроэкологии кишечника, дефиците бифидофлоры и лактобацилл, беспрепятственном бактериальном заселении тонкой и толстой кишки возникают условия для снижения не только местной защиты, но и резистентности организма в целом.
Несмотря на достаточную иммуногенность, сапрофитные микроорганизмы не вызывают реакций иммунной системы. Возможно, это происходит потому, что сапрофитная микрофлора является своего рода хранилищем микробных плазмидных и хромосомных генов, обмениваясь генетическим материалом с клетками хозяина. Реализуются внутриклеточные взаимодействия путем эндоцитоза, фагоцитоза и пр. При внутриклеточных взаимодействиях достигается эффект обмена клеточным материалом. В результате представители микрофлоры приобретают рецепторы и другие антигены, присущие хозяину. Это делает их «своими» для иммунной системы макроорганизма. Эпителиальные ткани в результате такого обмена приобретают бактериальные антигены.
Обсуждается вопрос о ключевом участии микрофлоры в обеспечении противовирусной защиты хозяина. Благодаря феномену молекулярной мимикрии и наличию рецепторов, приобретенных от эпителия хозяина, микрофлора становится способной к перехвату и выведению вирусов, обладающих соответствующими лигандами.
Таким образом, наряду с низким рН желудочного сока, двигательной и секреторной активностью тонкой кишки, микрофлора ЖКТ относится к неспецифическим факторам защиты организма.
Важной функцией микрофлоры является синтез ряда витаминов. Человеческий организм получает витамины в основном извне — с пищей растительного или животного происхождения. Поступающие витамины в норме всасываются в тонкой кишке и частично утилизируются кишечной микрофлорой. Микроорганизмы, населяющие кишечник человека и животных, продуцируют и утилизируют многие витамины. Примечательно, что наиболее важную роль для человека в этих процессах играют микробы тонкой кишки, так как продуцируемые ими витамины могут эффективно всасываться и поступать в кровоток, тогда как витамины, синтезирующиеся в толстой кишке, практически не всасываются и для человека оказываются недоступными. Подавление микрофлоры (например, антибиотиками) снижает и синтез витаминов. Наоборот, создание благоприятных для микроорганизмов условий, например при употреблении в пищу достаточного количества пребиотиков, повышает обеспеченность макроорганизма витаминами.
Наиболее изучены в настоящее время аспекты, связанные с синтезом кишечной микрофлорой фолиевой кислоты, витамина В12 и витамина К.
Фолиевая кислота (витамин В9), поступая с продуктами питания, эффективно всасывается в тонкой кишке. Синтезирующийся в толстой кишке представителями нормальной кишечной микрофлоры фолат идет исключительно для ее собственных нужд и не утилизируется макроорганизмом. Тем не менее синтез фолата в толстой кишке может иметь большое значение для нормального состояния ДНК колоноцитов.
Кишечные микроорганизмы, синтезирующие витамин В12, обитают как в толстой, так и в тонкой кишке. Среди этих микроорганизмов наиболее активны в данном аспекте представители Pseudomonas и Klebsiella sp. Однако возможностей микрофлоры для полной компенсации гиповитаминоза В12 оказывается недостаточно.
С содержанием в просвете толстой кишки фолата и кобаламина, полученных с пищей или синтезированных микрофлорой, связана способность эпителия кишечника противостоять процессам канцерогенеза. Предполагается, что одной из причин более высокой частоты опухолей толстой кишки, по сравнению с тонкой, является недостаток цитопротекторных составляющих, большинство из которых всасывается в средних отделах ЖКТ. Среди них — витамин В12 и фолиевая кислота, которые совместно определяют стабильность клеточных ДНК, в частности ДНК клеток эпителия толстой кишки. Даже незначительный дефицит этих витаминов, не вызывающий анемию или другие тяжелые последствия, тем не менее приводит к значимым аберрациям в молекулах ДНК колоноцитов, способным стать основой канцерогенеза. Известно, что недостаточное поступление к колоноцитам витаминов В6, В12 и фолиевой кислоты ассоциируется с повышенной частотой рака толстой кишки в популяции. Дефицит витаминов приводит к нарушению процессов метилирования ДНК, мутациям и, как следствие, раку толстой кишки. Риск толстокишечного канцерогенеза повышается при низком потреблении пищевых волокон и овощей, обеспечивающих нормальное функционирование кишечной микрофлоры, синтезирующей трофические и протективные в отношении толстой кишки факторы.
Витамин К существует в нескольких разновидностях и необходим человеческому организму для синтеза различных кальцийсвязывающих белков. Источником витамина К1, филохинона, являются продукты растительного происхождения, а витамин К2, группа соединений менахинонов, синтезируется в тонкой кишке человека. Микробный синтез витамина К2 стимулируется при недостатке филохинона в диете и вполне способен его компенсировать. В то же время недостаточность витамина К2 при сниженной активности микрофлоры плохо корригируется диетическими мероприятиями. Таким образом, синтетические процессы в кишечнике являются приоритетными для обеспечения макроорганизма этим витамином. Витамин К синтезируется и в толстой кишке, но используется преимущественно для потребностей микрофлоры и колоноцитов.
Кишечная микрофлора принимает участие в детоксикации экзогенных и эндогенных субстратов и метаболитов (аминов, меркаптанов, фенолов, мутагенных стероидов и др.) и, с одной стороны, представляет собой массивный сорбент, выводя из организма токсические продукты с кишечным содержимым, а с другой — утилизирует их в реакциях метаболизма для своих нужд. Помимо этого, представители сапрофитной микрофлоры продуцируют на основе конъюгатов желчных кислот эстрагеноподобные субстанции, оказывающие влияние на дифференцировку и пролиферацию эпителиальных и некоторых других тканей путем изменения экспрессии генов или характера их действия.
Итак, взаимоотношения микро- и макроорганизма носят сложный характер, реализующийся на метаболическом, регуляторном, внутриклеточном и генетическом уровне. Однако нормальное функционирование микрофлоры возможно только при хорошем физиологическом состоянии организма и в первую очередь нормальном питании.
Питание микроорганизмов, населяющих кишечник, обеспечивается за счет нутриентов, поступающих из вышележащих отделов ЖКТ, которые не перевариваются собственными ферментативными системами и не всасываются в тонкой кишке. Эти вещества необходимы для обеспечения энергетических и пластических потребностей микроорганизмов. Способность использовать нутриенты для своей жизнедеятельности зависит от ферментативных систем различных бактерий.
В зависимости от этого условно выделяют бактерии с преимущественно сахаролитической активностью, основным энергетическим субстратом которых являются углеводы (характерно в основном для сапрофитной флоры), с преимущественной протеолитической активностью, использующих белки для энергетических целей (характерно для большинства представителей патогенной и условно-патогенной флоры), и смешанной активностью. Соответственно, преобладание в пище тех или иных нутриентов, нарушение их переваривания будет стимулировать рост различных микроорганизмов.
Углеводные нутриенты особенно необходимы для жизнедеятельности нормальной кишечной микрофлоры. Ранее эти компоненты пищи называли «балластными», предполагая, что они не имеют какого-либо существенного значения для макроорганизма, однако по мере изучения микробного метаболизма стало очевидно их значение не только для роста кишечной микрофлоры, но для здоровья человека в целом. Согласно современному определению, пребиотиками называют частично или полностью не перевариваемые компоненты пищи, которые избирательно стимулируют рост и/или метаболизм одной или нескольких групп микроорганизмов, обитающих в толстой кишке, обеспечивая нормальный состав кишечного микробиоценоза. Свои энергетические потребности микроорганизмы толстой кишки обеспечивают за счет анаэробного субстратного фосфорилирования, ключевым метаболитом которого является пировиноградная кислота (ПВК). ПВК образуется из глюкозы в процессе гликолиза. Далее, в результате восстановления ПВК, образуется от одной до четырех молекул аденозинтрифосфата (АТФ). Последний этап приведенных выше процессов обозначается как брожение, которое может идти различными путями с образованием различных метаболитов.
Гомоферментативное молочное брожение характеризуется преимущественным образованием молочной кислоты (до 90%) и характерно для лактобактерий и стрептококков толстой кишки. Гетероферментативное молочное брожение, при котором образуются и другие метаболиты (в том числе уксусная кислота), присуще бифидобактериям. Спиртовое брожение, ведущее к образованию углекислого газа и этанола, является побочным метаболическим эффектом у некоторых представителей Lactobacillus и Clostridium. Отдельные виды энтеробактерий (E. coli) и клостридий получают энергию в результате муравьинокислого, пропионового, маслянокислого, ацетонобутилового или гомоацетатного видов брожения.
В результате микробного метаболизма в толстой кишке образуются молочная кислота, короткоцепочечные жирные кислоты (С2 — уксусная; С3 — пропионовая; С4 — масляная/изомасляная; С5 — валериановая/изовалериановая; С6 — капроновая/изокапроновая), углекислый газ, водород, вода. Углекислый газ в большой степени преобразуется в ацетат, водород всасывается и выводится через легкие, а органические кислоты (в первую очередь жирные короткоцепочечные) утилизируются макроорганизмом. Нормальная микрофлора толстой кишки, перерабатывая не переваренные в тонкой кишке углеводы, производит короткоцепочечные жирные кислоты с минимальным количеством их изоформ. В то же время при нарушении микробиоценоза и увеличении доли протеолитической микрофлоры указанные жирные кислоты начинают синтезироваться из белков преимущественно в виде изоформ, что отрицательно сказывается на состоянии толстой кишки, с одной стороны, и может быть диагностическим маркером — с другой.
Помимо этого, различные представители сапрофитной флоры имеют свои потребности в определенных нутриентах, объясняющиеся особенностями их метаболизма. Так, бифидобактерии расщепляют моно-, ди-, олиго- и полисахариды, используя их как энергетический и пластический субстрат. При этом они могут ферментировать белки, в том числе и для энергетических целей; не требовательны к поступлению с пищей большинства витаминов, но нуждаются в пантотенатах.
Лактобактерии также используют различные углеводы для энергетических и пластических целей, однако плохо расщепляют белки и жиры, поэтому нуждаются в поступлении извне аминокислот, жирных кислот, а также витаминов.
Энтеробактерии расщепляют углеводы с образованием углекислого газа, водорода и органических кислот. При этом существуют лактозонегативные и лактозопозитивные штаммы. Также они могут утилизировать белки и жиры, поэтому мало нуждаются во внешнем поступлении аминокислот, жирных кислот и большинства витаминов.
Очевидно, что питание сапрофитной микрофлоры и ее нормальное функционирование принципиально зависит от поступления к ней не переваренных углеводов (ди-, олиго- и полисахаридов) для энергетических целей, а также белков, аминокислот, пуринов и пиримидинов, жиров, углеводов, витаминов и минералов — для пластического обмена. Залогом поступления к бактериям необходимых нутриентов является рациональное питание макроорганизма и нормальное течение пищеварительных процессов.
Хотя моносахариды могут легко утилизироваться микроорганизмами толстой кишки, к пребиотикам их не относят.
В нормальных условиях кишечная микрофлора не потребляет моносахариды, которые должны полностью всасываться в тонкой кишке. Пребиотики включают некоторые дисахариды, олигосахариды, полисахариды и достаточно гетерогенную группу соединений, в которой присутствуют и поли- и олигосахариды, которую обозначили как пищевые волокна. Из пребиотиков в женском молоке присутствует лактоза и олигосахариды.
Лактоза (молочный сахар) представляет собой дисахарид, состоящий из галактозы и глюкозы. В норме лактоза расщепляется лактазой тонкой кишки до мономеров, которые практически полностью всасываются в тонкой кишке. Лишь незначительное количество нерасщепленной лактозы у детей первых месяцев жизни попадает в толстую кишку, где утилизируется микрофлорой, обеспечивая ее становление. В то же время дефицит лактазы приводит к избытку лактозы в толстой кишке и значительному нарушению состава кишечной микрофлоры и осмотической диарее.
Лактулоза — дисахарид, состоящий из галактозы и фруктозы, в молоке (женском или коровьем) отсутствует, однако в небольших количествах может образовываться при нагревании молока до температуры кипения. Лактулоза не переваривается ферментами ЖКТ, ферментируется лакто- и бифидобактериями и служит им субстратом для энергетического и пластического обмена, за счет чего способствует их росту и нормализации состава микрофлоры, увеличению объема биомассы в содержимом кишечника, что определяет ее слабительный эффект. Помимо этого, показана антикандидозная активность лактулозы и ее угнетающий эффект на сальмонелл. Полученная синтетическим путем лактулоза (дюфалак) широко используется как эффективное слабительное средство, обладающее пребиотическими свойствами. Как пребиотик детям дюфалак назначается в низких дозах, не оказывающих слабительного эффекта (по 1,5–2,5 мл 2 раза в день в течение 3–6 нед).
Олигосахариды представляют собой линейные полимеры глюкозы и других моносахаров с общей длиной цепи не более 10. По химической структуре выделяют галакто-, фрукто-, фукозил-олигосахариды и др. Концентрация олигосахаридов в женском молоке относительно невелика, не более 12–14 г/л, однако их пребиотический эффект весьма значителен. Именно олигосахариды сегодня рассматриваются как основные пребиотики женского молока, обеспечивающие как становление нормальной микрофлоры кишечника ребенка, так и ее поддержание в дальнейшем. Важным является то обстоятельство, что олигосахариды присутствуют в значимых концентрациях только в женском молоке и отсутствуют, в частности, в коровьем. Следовательно, в состав адаптированных молочных смесей для искусственного вскармливания здоровых детей должны добавляться пребиотики (галакто- и фруктосахариды).
Полисахариды представляют собой длинноцепочечные углеводы в основном растительного происхождения. Инулин, содержащий фруктозу, в больших количествах присутствует в артишоках, клубнях и корнях георгинов и одуванчиков; утилизируется бифидо- и лактобактериями, способствует их росту. Помимо этого, инулин повышает всасывание кальция и влияет на метаболизм липидов, снижая риск развития атеросклероза.
Пищевые волокна — большая гетерогенная группа полисахаридов, наиболее известными из которых являются целлюлоза и гемицеллюлоза. Целлюлоза — неразветвленный полимер глюкозы, а гемицеллюлоза — полимер глюкозы, арабинозы, глюкуроновой кислоты и ее метилового эфира. Помимо функции субстрата для питания лакто- и бифидофлоры и опосредованно поставщика короткоцепочечных жирных кислот для колоноцитов, пищевые волокна оказывают и другие важные эффекты. Они обладают высокой адсорбционной способностью и удерживают воду, что приводит к повышению осмотического давления в полости кишки, увеличению объема фекалий, ускорения пассажа по кишечнику, что обусловливает слабительный эффект.
В средних количествах (1–1,9 г/100 г продукта) пищевые волокна содержатся в моркови, сладком перце, петрушке (в корне и зелени), редьке, репе, тыкве, дыне, черносливе, цитрусовых, бруснике, фасоли, гречневой, перловой крупе, «Геркулесе», ржаном хлебе.
Высокое содержание (2–3 г/100 г продукта) пищевых волокон характерно для чеснока, клюквы, красной и черной смородины, черноплодной рябины, ежевики, овсяной крупы, хлеба из белково-отрубной муки.
Наибольшее же их количество (более 3 г/100 г) содержится в укропе, кураге, клубнике, малине, чае (4,5 г/100 г), овсяной муке (7,7 г/100 г), пшеничных отрубях (8,2 г/100 г), сушеном шиповнике (10 г/100 г), жареном кофе в зернах (12,8 г/100 г), овсяных отрубях (14 г/100 г). Пищевые волокна отсутствуют в рафинированных продуктах.
Несмотря на очевидную значимость пребиотиков для питания микрофлоры, благополучия ЖКТ и всего организма в целом, в современных условиях отмечается дефицит пребиотиков в питании во всех возрастных группах. В частности, взрослый человек должен съедать в сутки примерно 20–35 г пищевых волокон, тогда как в реальных условиях европеец потребляет не более 13 г в сутки. Уменьшение доли естественного вскармливания у детей первого года жизни приводит к недостатку пребиотиков, содержащихся в женском молоке.
Таким образом, пребиотики обеспечивают благополучие микрофлоры толстой кишки, здоровье толстой кишки и являются необходимым фактором здоровья человека в связи с их существенными метаболическими эффектами. Преодоление дефицита пребиотиков в современных условиях связано с обеспечением рационального питания лиц всех возрастных категорий, начиная от новорожденных и кончая людьми преклонного возраста.
Литература
С. В. Бельмер, доктор медицинских наук, профессор
А. В. Малкоч, кандидат медицинских наук
РГМУ, Москва