Фагоцитоз
Процесс активного захватывания и поглощения живых и неживых частиц одноклеточными организмами или особыми клетками (фагоцитами) многоклеточных животных организмов. Явление Ф. было открыто И. И. Мечниковым, который проследил его эволюцию и выяснил роль этого процесса в защитных реакциях организма высших животных и человека, главным образом при воспалении (См. Воспаление) и Иммунитете. Большую роль Ф. играет при заживлении ран. Способность захватывать и переваривать частицы лежит в основе питания примитивных организмов. В процессе эволюции эта способность постепенно перешла к отдельным специализированным клеткам, вначале пищеварительным, а затем – к особым клеткам соединительной ткани. У человека и млекопитающих животных активными фагоцитами являются Нейтрофилы (микрофаги, или специальные лейкоциты) крови и клетки ретикуло-эндотелиальной системы (См. Ретикуло-эндотелиальная система), способные превращаться в активных макрофагов (См. Макрофаги). Нейтрофилы фагоцитируют мелкие частицы (бактерии и т.п.), макрофаги способны поглощать более крупные частицы (погибшие клетки, их ядра или фрагменты и т.п.). Макрофаги способны также накапливать отрицательно заряженные частицы красителей и коллоидных веществ. Поглощение мелких коллоидных частиц называют ультрафагоцитозом, или коллоидопексией.
Ф. требует затраты энергии и связан прежде всего с активностью клеточной мембраны и внутриклеточных органоидов – лизосом, содержащих большое количество гидролитических ферментов. В ходе Ф. различают несколько стадий. Вначале фагоцитируемая частица прикрепляется к клеточной мембране, которая затем обволакивает её и образует внутриклеточное тельце – фагосому. Из окружающих лизосом в фагосому попадают гидролитические ферменты, переваривающие фагоцитируемую частицу. В зависимости от физико-химических свойств последней переваривание может быть полным или неполным. В последнем случае образуется остаточное тельце, которое может оставаться в клетке длительное время.
Лит.: Мечников И. И., Избранные биологические произведения, М., 1950; Зильбер Л. А., Основы иммунологии, 3 изд., М., 1958.
Фагоцитоз что это биология
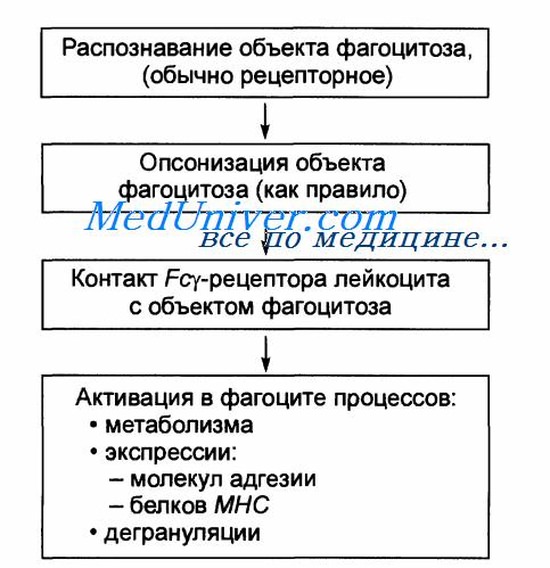
Наиболее важной функцией нейтрофилов и макрофагов является фагоцитоз — поглощение клеткой вредоносного агента. Фагоциты избирательны в отношении материала, который они фагоцитируют; иначе они могли бы фагоцитировать нормальные клетки и структуры организма. Осуществление фагоцитоза зависит главным образом от трех специфических условий.
Во-первых, большинство естественных структур имеют гладкую поверхность, которая препятствует фагоцитозу. Но если поверхность неровная, возможность фагоцитирования возрастает.
Во-вторых, большинство естественных поверхностей имеют защитные белковые оболочки, отталкивающие фагоциты. С другой стороны, большинство погибших тканей и инородных частиц лишены защитных оболочек, что делает их объектом фагоцитоза.
В-третьих, иммунная система организма образует антитела против инфекционных агентов, например бактерий. Антитела прикрепляются к мембранам бактерий, и бактерии становятся особенно чувствительными к фагоцитозу. Для осуществления этой функции молекула антитела также соединяется с продуктом С3 каскада комплемента — дополнительной частью иммунной системы, обсуждаемой в отдельной статье на сайте (просим вас пользоваться формой поиска выше). Молекулы С3, в свою очередь, прикрепляются к рецепторам на мембране фагоцитов, инициируя фагоцитоз. Этот процесс выбора и фагоцитоза называют опсонизацией.
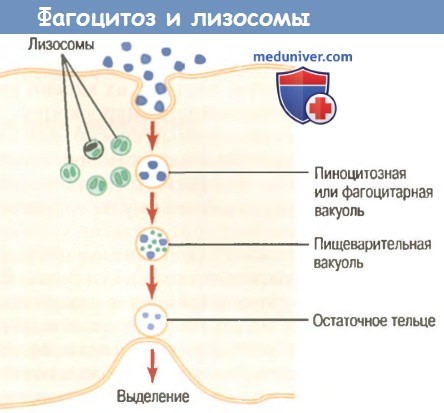
а) Фагоцитоз, осуществляемый нейтрофилами. Нейтрофилы, входящие в ткани, являются уже зрелыми клетками, способными к немедленному фагоцитозу. При встрече с частицей, которая должна быть фагоцитирована, нейтрофил сначала прикрепляется к ней, а затем выпускает псевдоподии во всех направлениях вокруг частицы. На противоположной стороне частицы псевдоподии встречаются и сливаются друг с другом. При этом образуется замкнутая камера, содержащая фагоцитируемую частицу. Затем камера погружается в цитоплазматическую полость и отрывается от наружной стороны клеточной мембраны, формируя свободно плавающий фагоцитарный пузырек (также называемый фагосомои) внутри цитоплазмы. Один нейтрофил обычно может фагоцитировать от 3 до 20 бактерий, прежде чем он сам инактивируется или погибает.
б) Фагоцитоз, осуществляемый макрофагами. Макрофаги представляют собой конечную стадию развития моноцитов, входящих в ткани из крови. При активации иммунной системой они становятся гораздо более мощными фагоцитами, чем нейтрофилы, и часто могут фагоцитировать до 100 бактерий. Макрофаги также способны поглощать гораздо более крупные частицы, даже целые эритроциты и иногда малярийных паразитов, тогда как нейтрофилы не могут фагоцитировать частички, размер которых значительно превышает размер бактерии. Кроме того, макрофаги могут выталкивать конечные продукты и часто живут и функционируют в течение многих месяцев.
в) Сразу после фагоцитирования большинство частиц перевариваются внутриклеточными ферментами. После фагоцитирования инородной частицы лизосомы и другие цитоплазматические гранулы нейтрофила или макрофага немедленно вступают в контакт с фагоцитарным пузырьком, их мембраны сливаются, в результате в пузырек вбрасываются многие переваривающие ферменты и бактерицидные вещества. Таким образом, фагоцитарный пузырек теперь становится переваривающим пузырьком, и сразу начинается расщепление фагоцитированной частицы.
И нейтрофилы, и макрофаги содержат громадное количество лизосом, наполненных протеолитическими ферментами, особенно приспособленными для переваривания бактерий и других чужеродных белковых веществ. Лизосомы макрофагов (но не нейтрофилов) содержат также большое количество липаз, которые разрушают толстые липидные мембраны, покрывающие некоторые бактерии, например туберкулезную палочку.
Однако некоторые бактерии, особенно туберкулезная палочка, имеют оболочки, устойчивые к лизосомальному перевариванию, и к тому же секретируют вещества, отчасти препятствующие «убивающим» эффектам нейтрофилов и макрофагов. Такие бактерии ответственны за многие хронические болезни, например туберкулез.
Видео стадии фагоцитоза и питание клетки
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»
Фагоцитоз
Фагоцито́з (др.-греч. φαγεῖν — пожирать и κύτος — клетка) — процесс, при котором специально предназначенные для этого клетки крови и тканей организма (фагоциты) захватывают и переваривают твёрдые частицы. Осуществляется двумя разновидностями клеток: циркулирующими в крови зернистыми лейкоцитами (гранулоцитами) и тканевыми макрофагами. Открытие фагоцитоза принадлежит И. И. Мечникову, который выявил этот процесс, проделывая опыты с морскими звёздами и дафниями, вводя в их организмы инородные тела. Например, когда Мечников поместил в тело дафнии спору грибка, то он заметил, что на неё нападают особые подвижные клетки. Когда же он ввёл слишком много спор, клетки не успели их все переварить, и животное погибло. Клетки, защищающие организм от бактерий, вирусов, спор грибов и пр., Мечников назвал фагоцитами.
У человека различают два типа профессиональных фагоцитов:
Основные этапы фагоцитарной реакции сходны для клеток обоих типов. Реакция фагоцитоза может быть подразделена на несколько этапов:
1. Хемотаксис. В реакции фагоцитоза более важная роль принадлежит положительному хемотаксису. В качестве хемоаттрактантов выступают продукты выделяемые микроорганизмами и активированными клетками в очаге воспаления (цитокины, лейкотриен В4, гистамин), а также продукты расщепления компонентов комплемента (С3а, С5а), протеолитические фрагменты факторов свертывания крови и фибринолиза (тромбин, фибрин), нейропептиды, фрагменты иммуноглобулинов и др. Однако, «профессиональными» хемотаксинами служат цитокины группы хемокинов.
Ранее других клеток в очаг воспаления мигрируют нейтрофилы, существенно позже поступают макрофаги. Скорость хемотаксического перемещения для нейтрофилов и макрофагов сопоставима, различия во времени поступления, вероятно, связаны с разной скоростью их активации.
2. Адгезия фагоцитов к объекту. Обусловлена наличием на поверхности фагоцитов рецепторов для молекул, представленных на поверхности объекта (собственных или связавшихся с ним). При фагоцитозе бактерий или старых клеток организма хозяина происходит распознавание концевых сахаридных групп — глюкозы, галактозы, фукозы, маннозы и др., которые представлены на поверхности фагоцитируемых клеток. Распознавание осуществляется лектиноподобными рецепторами соответствующей специфичности, в первую очередь маннозосвязывающим белком и селектинами, присутствующими на поверхности фагоцитов.
В тех случаях, когда объектами фагоцитоза являются не живые клетки, а кусочки угля, асбеста, стекла, металла и др., фагоциты предварительно делают объект поглощения приемлемым для осуществления реакции, окутывая его собственными продуктами, в том числе компонентами межклеточного матрикса, который они продуцируют.
3. Активация мембраны. На этой стадии осуществляется подготовка объекта к погружению. Происходит активация протеинкиназы С, выход ионов кальция из внутриклеточных депо. Большое значение играют переходы золь-гель в системе клеточных коллоидов и актино-миозиновые перестройки.
4. Погружение. Происходит обволакивание объекта.
5. Образование фагосомы. Замыкание мембраны, погружение объекта с частью мембраны фагоцита внутрь клетки.
6. Образование фаголизосомы. Слияние фагосомы с лизосомами, в результате чего образуются оптимальные условия для бактериолиза и расщепления убитой клетки. Механизмы сближения фагосомы и лизосом неясны, вероятно имеется активное перемещение лизосом к фагосомам.
7. Киллинг и расщепление. Велика роль клеточной стенки перевариваемой клетки. Основные вещества участвующие в бактериолизе: перекись водорода, продукты азотного метаболизма, лизоцим и др. Процесс разрушения бактериальных клеток завершается благодаря активности протеаз, нуклеаз, липаз и других ферментов, активность которых оптимальна при низких значениях pH.
8. Выброс продуктов деградации.
Фагоцитоз может быть:
Что такое фагоциты и какова их роль в организме

Общая характеристика фагоцитов
Фагоцитоз был впервые описан русским ученым Ильей Ильичем Мечниковым более 100 лет тому назад. Ученый, наблюдая за плоскими червями и личинками морских звезд, обнаружил у них удивительное свойство: не имея рта, они способны поглощать и растворять разные вещества. В ходе наблюдения биолог предположил, что это свойство особых клеток, которые содержатся в этих организмах. Оказалось, что эти клетки быстро перемещаются внутри личинок и поглощают все, что попадает в организм. Причем выявленные клетки способны поглощать не только пищу. Мечников вонзил в тельце личинки морской звезды маленькую деревянную занозу и начал наблюдать в микроскоп за поведением удивительных клеток. Вскоре они скопились вокруг занозы и начали ее пожирать. Эти «прожорливые» клетки и есть фагоциты, их название происходит от греческих слов, которые так и переводятся – «пожирать».
В ходе дальнейших исследований было обнаружено, что фагоциты продуцируются костным мозгом, содержатся в организме всех животных и человека, концентрируются в крови и почти всех тканях, в нашем организме они представлены в нескольких видах.
Как «работают» фагоциты в человеческом организме
Фагоциты защищают организм от бактерий, токсических веществ и некоторых вирусов, способны продуцировать разные биоактивные вещества, стимулировать воспалительные реакции, а также активизировать работу других агентов иммунной системы. По сути, фагоциты – это вторая линия защиты организма от патогенов, которые все же проникли в организм. Процесс поглощения фагоцитарными клетками опасных для человека агентов называется фагоцитозом.
Для упрощенного понимания механизмов фагоцитоза следует вспомнить амебу – представителя одноклеточных, известного большинству со школьной программы. Как и амеба, фагоцит имеет так называемые ложные ножки, которыми обволакивает свою добычу и поглощает ее. Сообщается о филогенетическом родстве амебы и фагоцитов.
При попадании в организм патогена рецепторы фагоцитов улавливают высвобождаемые им химические вещества и направляются к ним. При связывнии мишени с рецепторами фагоцита осуществляется фагоцитоз и чужеродный для организма агент разрушается индуцируемыми фагоцитами окислителями или оксидом азота. Остатки «съеденного» патогена выбрасываются обратно на поверхность фагоцита и элиминируются из организма.
Однако существуют факторы инвазивности, при которых патогены могут не только уклоняться от распознавания иммунной системой, но и управлять иммунными процессами. На ранних этапах инфицирования происходит взаимодействие патогенов с факторами врожденного иммунитета, и это является основным этапом для выживания возбудителей. Для того, чтобы ускользнуть от распознавания рецепторами фагоцитов патогенные бактерии используют следующие механизмы: прикрывают свою поверхность белками хозяина, образуют капсулы, варьируют молекулярными структурами клеточной стенки и др. Такие фагоцитированные бактерии могут выживать и размножаться внутри фагоцита, тем самым блокировать созревание фагосомы и воздействовать на внутриклеточные сигнальные пути.
Виды фагоцитов

Профессиональные фагоциты
Профессиональные фагоцитарные клетки характеризуются более узкой специализацией, то есть они взаимодействуют с определенной категорией мишеней. К профессиональным фагоцитам относятся моноциты, макрофаги, нейтрофилы, дендритные и тучные клетки. Эта группа считается особо важной для защиты организма.
Моноциты
Мононуклеарные фагоциты, или моноциты, представляют собой самые большие клетки среди лейкоцитов (белых кровяных клеток). На наружной стороне плазматической мембраны моноцитов локализовано множество рецепторов, число которых увеличивается по мере созревания моноцитов. Среди них имеются рецепторы к разным веществам, которые связывают JgG и иммунные комплексы; обеспечивают способность мононуклеарных клеток к фагоцитозу бактерий и различных клеток. В кровоток моноциты попадают из костного мозга, в котором они синтезируются. Эти клетки довольно быстро передвигаются и в сосудах остаются всего лишь от 24 до 48 часов, после чего проникают в другие ткани и превращаются в макрофаги.
Концентрация моноцитов в крови варьируется зависимо от возраста и регулируется балансом стимуляторов и ингибиторов. Повышение количества может быть признаком:
Недостаточное количество клеток из этой группы может быть связано с иммунными расстройствами – как врожденными, так и приобретенными (например, СПИД, атрофия костного мозга).
Макрофаги

Нейтрофилы
Нейтрофилы, как и моноциты, являются представителями группы клеток-лейкоцитов. В кровотоке на долю нейтрофилов приходится от 50% до 75% всех лейкоцитов. Продолжительность жизни нейтрофила составляет около 5 суток. Их основная задача – предотвратить развитие инфекции.
Современные лабораторные методы позволяют определять количество нейтрофилов в организме. Снижение их количества отмечается при таких заболеваниях, как:
Дефицит нейтрофилов также может быть вызван приемом некоторых лекарств, например, антибиотиков или диуретиков. Снижение лейкоцитов, в том числе и нейтрофилов, отмечается у онкологических пациентов, проходящих лучевую или химиотерапию.
Существенное повышение количества нейтрофилов может указывать на следующие заболевания:
Дендритные клетки
Свое название дендритные клетки получили из-за специфического строения. Они имеют множество разветвленных отростков, которые напоминают крону дерева (dendron). Клетки из этой группы в больших количествах содержатся в разных тканях, их основное количество концентрируются в полостях органов, а также в близости к внешней среде, то есть в слизистых оболочках носа, желудка, в альвеолярных тканях легких. После полного созревания дендритные клетки проникают в лимфоидную ткань (лимфоузлы, миндалины, серозную оболочку, носоглотку) и усиливают активность лимфоцитов и макрофагов.
Тучные клетки (лаброциты)
Главная задача лаброцитов – активизировать воспалительные реакции в организме, которые являются сигналом для макрофагов, нейтрофилов и других фагоцитов и должны защитить организм от внешнего возбудителя. Любое воспаление – это своеобразная команда к действию для всех присутствующих в организме фагоцитов. То есть лаброциты повышают активность разных групп фагоцитарных клеток и выполняют незаменимые функции, от которых зависит работа всей иммунной системы. Но сами тучные клетки также не лишены фагоцитарной активности. Они, как правило, специализируются на грамотрицательных бактериях.
Непрофессиональные фагоциты
Непрофессиональные фагоциты лишены направленного действия против конкретного вида патогена. Их фагоцитарная активность не столь выражена, как у профессиональных клеток. К этой группе принадлежат фибробласты, а также клетки эндотелия сосудов и эпителия. Они реагируют на любой патоген, проникший в организм.
Функции фагоцитов
Фагоциты – незаменимое звено иммунной системы. Анализируя главные характеристики разных типов фагоцитарных клеток, можно решить, что их основная задача – защищать от инфекции. Но это далеко не единственная их функция. Они «пожирают» (процесс фагоцитоза) твердые частицы, которые в человеческом организме являются патогенными, очищают кровь, поддерживают здоровье внутренних органов и выполняют еще множество полезных функций.
1. Защита от чужеродных тел

2. Защита от опухолей
Известно, что в результате множества подтвержденных и подозреваемых факторов в организме человека происходят нарушения, которые приводят к неконтролируемому делению и росту клеток, который может быть как доброкачественного, так и злокачественного характера. Иммунная система играет важную роль в противоопухолевой защите: фагоциты немедленно отыскивают перерожденные клетки и уничтожают их, предотвращая таким образом онкологические заболевания.
3. Участие в процессе апоптоза
В среднем организм взрослого человека – это примерно 100 триллионов клеток, среди которых некоторые живут несколько суток, другие являются «долгожителями» и живут по несколько лет. Ежедневно гибнет около 70 миллиардов клеток, которые удаляют макрофаги. При естественной гибели клеток, они выделяют некие вещества, на которые реагируют фагоциты и уничтожают старые клетки. Этот процесс называется апоптозом.
4. Защита от болезней
Фагоцитарные образования способны предотвращать заболевания, которые не связаны с инфекцией, опухолью или другими факторами, интересными для фагоцитов. Например, при атеросклерозе макрофаги участвуют в замедлении прогрессии заболевания. Когда холестерин откладывается в эндотелии сосудов, макрофаги «поедают» частицы жира и вместо него образуются так называемые пенистые клетки. Но фагоцитарные клетки не способны полностью уничтожать липопротеины, поэтому холестериновые бляшки продолжают образовываться на стенках сосудов, хотя в некоторых случаях и несколько медленнее.
5. Поддержка функций иммунной системы
Фагоцитарные клетки обладают способностью повышать активность друг друга, а также других агентов иммунной системы. Кроме того, фагоциты выделяют специфические вещества, которые стимулируют костный мозг на выработку клеток иммунной системы.
6. Способствуют восстановлению тканей
Фагоциты также могут участвовать в формировании тканей при их повреждении за счет образования рубцовых клеток (фибробластов). В результате в месте повреждения появляется «латка» в виде рубца. Этот процесс происходит не только при внешних повреждениях кожи. Фибробласты незаменимы для рубцевания язвы органов ЖКТ и заживления миокарда в постинфарктный период.
Всегда ли фагоциты полезны
Механизм воздействия на патогены у фагоцитов отработан тысячелетиями эволюции. Но даже это не делает их абсолютно безопасными и полезными для человеческого организма. И во многом виной являются не столько сами фагоциты, сколько условия современной жизни человека. Плохая экология, хронические стрессы часто приводят к тому, что в принципах работы фагоцитов появляются сбои. Взять хотя бы аутоиммунные заболевания. Эта группа болезней вызвана тем, что вследствие сбоя иммунитет воспринимает клетки собственного организма как патогены. Как следствие, фагоциты «набрасываются» на ткани почек, суставы, разные части сердца, и организм начинает стареть в несколько раз быстрее.
В человеческом организме присутствует огромное количество клеток специфического действия – фагоцитов. Они взаимодействуют между собой и другими клетками, поэтому очень важно обеспечение нормального протекания этого процесса. Любой дисбаланс этого взаимодействия влечет за собой проблемы со здоровьем. Лучшая помощь для оптимального функционирования системы фагоцитоза – это соблюдение здорового образа жизни, правильного питания и поддержания иммунитета в норме.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
ФАГОЦИТОЗ
Объектом фагоцитоза являются микробы, чужеродные и измененные собственные клетки или их фрагменты, комплексы антиген — антитело и др. Неотъемлемую часть фагоцитоза составляет направленное движение — хемотаксис (см. Таксисы) — фагоцитов к месту локализации чужеродной частицы.
Определение эффективности фагоцитоза проводится для оценки состояния иммунобиологической реактивности организма, а также при различных медико-биологических исследованиях.
Явление фагоцитоза как биологической универсальной реакции одноклеточных, многоклеточных и высших организмов было открыто И. И. Мечниковым, который в 1883 году сформулировал теорию фагоцитоза. И. И. Мечников рассматривал фагоцитоз как одну из форм питания клеток (начиная с простейших). У высокоорганизованных организмов эта форма питания свойственна особым мезенхимальным клеткам-фагоцитам поглощающим и убивающим патогенные микробы и таким образом выполняющим защитную функцию. Именно с функцией этих клеток И. И. Мечников связывал иммунитет к возбудителям инфекционных болезней. Им были описаны фазы фагоцитарного процесса и состояние активации фагоцитов, характеризующееся их новыми свойствами и усиленной способностью поглощать и уничтожать бактерии. Ключевая роль фагоцитов была доказана им в иммунитете, при воспалении, удалении поврежденных клеток, регенерации, атрофии, старении.
Опсонизированные и неопсонизированные частицы прикрепляются к фагоцитам также с помощью специфических Fc-рецепторов для IgE, гликопротеидов и полисахаридов и неспецифических рецепторов для чужеродных веществ. Большинство нейтрофилов человека содержат Fc-рецепторы для агрегированного IgGl и IgG3, а возможно и для агрегированного I g А; моноциты — рецепторы для IgGl и IgG3. Рецепторы для комплемента высокоаффинны (обладают высокой прочностью соединения), они обеспечивают прилипание опсонизированных частиц к неактивированным макрофагам, поглощают же такие частицы только активированные клетки. На нейтрофилах найдены рецепторы для C3b-, C4b- и C5a-субкомпонентов комплемента, на макрофагах — один рецептор для C3b- и C4b-, другой — для C3b- и C3c1-субкомпонентов комплемента. Если частица опсонизирована иммуноглобулином и комплементом, связывание с фагоцитом осуществляется кооперативно через специфические к ним рецепторы, что значительно активирует ее поглощение. Имеются различия между классами рецепторов и опосредуемыми ими реакциями фагоцитоза. Посредством неспецифических и специфических для гликопротеидов и полисахаридов рецепторов осуществляется фагоцитоз бактерий без опсонинов. Известен фагоцитоз инертных частиц — кремнезема, угля и др.
Опсонины не только прикрепляют объект фагоцитоза к поверхности фагоцитов, но и активируют их, индуцируя сигналы, идущие от плазматической мембраны, опосредованно вызывают активацию разных гуморальных систем организма, усиливая фагоцитоз.
Процесс поглощения опсонизированной частицы начинается с взаимодействия рецепторов фагоцита с опсонинами, локализованными на поверхности частицы. В дальнейшем происходит взаимодействие соседних свободных рецепторов фагоцита с близлежащими свободными опсонинами частицы до тех пор, пока не будут связаны все опсонины, покрывающие частицу на периферии, и она полностью не погрузится в цитоплазму фагоцита вместе с окружающим участком плазматической мембраны, образуя фагосому. Взаимодействие частицы с плазматической мембраной фагоцита посредством образующихся комплексов опсонин-рецептор запускает сложный механизм фагоцитоза, основная роль в котором принадлежит работе сократительных белков. Процесс поглощения начинается с образования псевдоподии — вытягивания участка цитоплазмы фагоцита в направлении частицы. При формировании псевдоподии находящиеся в ней неориентированные актиновые нити (филаменты) становятся параллельными, что сопровождается преходящим изменением вязкости цитоплазмы. Сформулирована гипотеза жесткости (желатинизации) — сокращения цитоплазмы, изменяющего ее состояние и генерирующего механическую силу движения фагоцита, регулируемого ионами кальция. При желатинизации актиновые нити перекрестно связываются актинсвязывающим белком, превращающим цитоплазму в гель вследствие образования актиновой решетки. Этот процесс подавляется особым кальцийзависимым актин-регуляторным белком — гельсолином, являющимся физиологическим регулятором желатинизации актина. Далее миозин образует перекрестные мостики с актином и гель начинает сокращаться, особенно в присутствии ионов магния, АТФ и кофактора, являющегося киназой, фосфорилирующей тяжелую цепь миозина. В месте контакта плазматической мембраны и частицы возрастает жесткость цитоплазматических структур (желатинизация участка цитоплазмы). Процесс идет непрерывно; постоянно из плазматической мембраны выделяется растворимый актинсвязывающий белок и мембрана движется по направлению к частице. В области прилипания частицы к плазматической мембране возрастает концентрация ионов кальция, которые «растворяют» актиновую решетку, снижают в этом участке жесткость цитоплазмы, и она движется в сторону повышенной жесткости на конце псевдоподии, т. к. нити миозина натягивают актиновые нити в направлении области наибольшей жесткости решетки.
В процессе фагоцитоза у нейтрофилов потребляется энергия, запасенная в виде АТФ, образованной в результате реакции гликолиза (см.). У альвеолярных макрофагов энергия для фагоцитоза в большей степени (возможно, в основном) извлекается из АТФ, образованной в процессе окислительного фосфорилирования (см. Окисление биологическое). Установлено, что метаболическим показателем в макрофагах является не абсолютное содержание АТФ, а скорость обновления. Количество АТФ в фагоцитирующих макрофагах частично поддерживается путем фосфорилирования АДФ за счет креатинфосфата (см. Креатин), которого в макрофагах в 3—5 раз больше, чем АТФ, и потребление существенно возрастает при фагоцитозе. Креатинфосфат в макрофагах служит, таким образом, важнейшим резервом и поставщиком химической энергии для фагоцитоза.
После завершения поглощения частицы возникшая фагосома и первичные лизосомы (см.), первичные азурофильные и вторичные специфические гранулы фагоцитов взаимно сближаются и сливаются, образуя фаголизосому. Этот процесс сопровождается исчезновением в фагоцитах изолированных гранул. Из лизосом в фагосому попадает большое количество гидролитических ферментов. Фагоцитоз также связан с секрецией из фагоцитов ряда ферментов — бета-глюкуронидазы, N-ацетил-бета-глюкозаминидазы, кислой и щелочной фосфатазы, катепсина, миелопероксидазы, лактоферрина, плазминогенного активатора. Подобная секреция сопряжена с активацией гексозомонофосфатного шунта и длится значительно дольше, чем непосредственно процесс фагоцитоза.
После проникновения бактерий внутрь фагоцитов начинает функционировать сложный микробоцидный механизм, представленный антимикробными системами, как требующими кислорода, так и не зависящими от него. Антимикробная система, требующая кислорода, функционирует в двух вариантах — с участием и без участия миелопероксидазы. Вариант с участием миелопероксидазы высокоактивен в отношении бактерий, грибков, микоплазм и вирусов. Взаимодействие миелопероксидазы и перекиси водорода сопровождается образованием окислителей, окислением галоидов и галогенизацией, заключающейся в иодировании, хлорировании, бронировании различных бактериальных компонентов, что приводит к гибели бактерий. При описанных реакциях образуются бактерицидные ионы хлора, йода, хлорамины, нитриты, бактерицидные альдегиды, синглетный кислород, которые блокируют многие ферментные системы бактерий. Не зависящий от миелопероксидазы вариант аштшикробной системы фагоцитов вызывает образование токсичных для микробов промежуточных форм восстановленного кислорода — супероксидного аниона, перекиси водорода, гидроксильного радикала и синглетного кислорода. Наиболее активна из них перекись водорода.
К антимикробной системе фагоцитоза, не зависящей от кислорода, относят: лизоцим (см.), расщепляющий пептидогликаны клеточных стенок некоторых грамположительных бактерий до дисахаридов, состоящих из мураминовой кислоты и глюкозамина; лактоферрин, который в ненасыщенной железом форме оказывает микробостатическое действие в фагосомах за счет связывания железа, являющегося ростовым фактором для ряда из них; различные катионные белки. Определенное бактерицидное действие оказывает также формирующееся в фаголизосомах глубокое закисление до pH 6,5—3,75.
Закисление, кроме того, активирует лизосомальные гидролазы первичных лизосом, неактивные при слабощелочном pH.
Микробоцидные системы фагоцитов функционируют в кооперации. Они обладают различной потенцией, но все вместе оказывают взаимоперекрывающее действие, поэтому обладают высокой надежностью и эффективностью даже при дефектах фагоцитоза.
При нарушении хемотаксиса фагоцитоз бактерий подавлен, что способствует развитию и злокачественному течению ряда инфекционных болезней. Вещества, индуцирующие хемотаксис, называются хемоаттрактантами и подразделяются на несколько групп: 1) продукты специфических, в основном иммунологических реакций,— СЗа-, С5а-субкомпоненты комплемента, активированный комплекс G567, СЗ-конвертаза альтернативного пути активации комплемента, лимфокины (см. Медиаторы клеточного иммунитета), трансферфактор лимфоцитов, цитофильные антитела; 2) неспецифические эндогенные хемо-аттрактанты — продукты поврежденных клеток, калликреин (см. Кинины), плазминогенный активатор, фибринопептид В, гидролизованные или агрегированные IgG, коллаген, а- и Р-казеин молока, циклический аденозинмонофосфат и др.; 3) экзогенные хемоаттрактанты — фрагменты белка бактерий, содержащие N-формилметионин, пептиды, липиды или липопротеиды, выделяющиеся в процессе жизнедеятельности бактерий в организме.
На поверхности фагоцитов обнаружены специфические рецепторы для хемоаттрактантов — эйкозатетраеновой кислоты, синтетических формил-метионил-пептидов, С5а-субкомпонента комплемента. По-видимому, число этих рецепторов неодинаково у разных типов фагоцитов, напр, циркулирующие нейтрофилы кролика в 8 раз слабее связывали хемотаксические пептиды, чем перитонеальные нейтрофилы. Доказана реакция сократительной системы клетки на действие хемоаттрактантов. Ее ориентация на градиент хемоаттрактантов обусловлена работой микротрубочек, выполняющих роль цитоскелета клетки,— они поддерживают поляризованную вытянутую на градиент хемоаттрактантов форму клетки. Однако непосредственно движение фагоцита осуществляет система микрофиламентов. Предполагают, что белки крови — альбумин и IgG являются регуляторами локомоторной функции фагоцитов. Активация фагоцитов хемоаттрактантами во многом сопровождается теми же изменениями, которые происходят при фагоцитозе — метаболическим взрывом, секрецией из клеток ферментов и др. Определенная регулирующая роль принадлежит циклическим нуклеотидам: циклический аденозинмонофосфат подавляет, а циклический гуанозинмонофосфат стимулирует хемотаксис.
Способы и методические подходы к оценке фагоцитоза разнообразны и зависят от конкретных задач исследования. Они позволяют определить эффективность процессов поглощения частиц, гибели и переваривания живых микроорганизмов и метаболические изменения фагоцитов. Важные данные о фагоцитозе могут быть также получены при исследовании хемотаксиса и опсонизации.
Для оценки фагоцитоза используют различные микроорганизмы — стафилококки (см.), эшерихии (см.), сальмонеллы (см. Сальмонелла) и др. Используют как живые, так и убитые микробы, но поскольку живые бактерии нередко выделяют токсические продукты, подавляющие фагоцитоз, лучше использовать убитые.
Фагоцитоз усиливается в присутствии сыворотки, опсонизирующей бактерии. Для усиления и стандартизации фагоцитоза используют предопсонизацию, то есть предварительную (до фагоцитоза) обработку микроба опсонинами — специфическими антителами — либо свежей сывороткой, в которой микробы активируют систему комплемента и адсорбируют появляющиеся субкомпоненты комплемента, облегчающие фагоцитоз. Однако в экспериментах с живыми микробами применяют лишь те, которые не убиваются опсонизирующей сывороткой. Скорость фагоцитоза анализируют при совместном инкубировании фагоцитов и живых бактерий. Через разные промежутки времени забирают пробы, с помощью дифференциального центрифугирования освобождаются от фагоцитов и надосадочную жидкость сеют на чашки с агаром, что позволяет определить уменьшение числа живых бактерий в процессе фагоцитоза. При работе с грибками рода Candida препарат просчитывают в камере Горяева, определяя при этом число внеклеточно расположенных грибков.
Для анализа фагоцитоза путем определения процента фагоцитов, поглотивших бактерии (фагоцитарный индекс Гамбургера), или среднего числа бактерий, поглощенных одним фагоцитом (фагоцитарное число Райга), скорости фагоцитоза используют частицы латекса, крахмала, зимозана, кармина, угля и др. Предложен метод исследования фагоцитоза, при котором используют капельки парафинового масла, содержащего специальный краситель и стабилизированного белком. Поглощенный материал определяют спектрофотометрически (см. Спектрофотометрия). Также используют частицы или микробы, меченные радиоактивными изотопами (см. Меченые соединения). Метод характеризуется быстротой выполнения, однако не позволяет полностью избавиться от прилипших бактерий, что завышает показатели фагоцитоза. Другой вариант состоит в добавлении к среде с фагоцитами и частицами меченых сывороточных белков, которые при фагоцитозе попадают в фагосому, что позволяет оценить количественно интенсивность фагоцитоза. Применяют также ксеногенные интактные или сингенные поврежденные или опсонизированные эритроциты, анализируя их поглощение визуально или по выходу гемоглобина.
При исследовании поглощения живых бактерий, особенно с последующим учетом количества убитых бактерий необходимо удалить с поверхности фагоцитов прилипшие микробы. Для этого применяют различные антибиотики, убивающие внеклеточные бактерии, но не проникающие в фагоциты, специальные препараты (фенилбутазан), прерывающие в определенные моменты фагоцитоза и внутриклеточную инактивацию микробов. Разработан метод, позволяющий различать прилипшие и поглощенные убитые грибки рода Candida по окраске препарата трипановым синим.
Гибель и переваривание поглощенных микробов выявляют путем инкубирования суспензии фагоцитов с микробами, последующего отмывания фагоцитов of прилипших микробных клеток, подсчета живых микробов, оставшихся в пробах фагоцитов, забираемых в различные сроки инкубации. Число живых бактерий определяют серийными посевами из проб фагоцитов на чашки Петри с агаром. Число живых грибков подсчитывают в лизате фагоцитов после инкубации с помощью окрашивания метиленовым синим. Внутриклеточное переваривание бактерий изучают также с помощью включения в них 3H-уридина. Для этого культуру фагоцитов, поглотивших бактерии, обрабатывают актиномицином D, добавляя в среду 3H-уридин. Метка, включаясь в живые внутриклеточные бактерии, не попадает в убитые и фагоциты.
Анализ повреждающего действия фагоцитов на микробы можно проводить по степени окрашивания поглощенных микробов красителями или по окраске метиленовым синим фаголизосом фагоцитов. Завершенность фагоцитоза оценивают по отношению среднего числа убитых микробов к живым или числа фагоцитов с переваренными микробами к общему числу фагоцитирующих фагоцитов, а также по проценту разрушенных микробов от числа фагоцитированных или по среднему числу убитых микробов на один фагоцит. Выраженность метаболических изменений при фагоцитозе анализируют по потреблению кислорода, хемилюминесценции, окислению глюкозы, иодированию и др.
Фагоциты играют ключевую роль в формировании противомикробного иммунитета (см. Иммунитет), обусловленного как специфическими, так и неспецифическими факторами защиты. Несмотря на то, что специфический иммунитет опосредуется специфическими Т-клетками, а также специфическими антителами, опсонизирующими бактерии и усиливающими фагоцитоз, элиминация патогенных бактерий осуществляется неспецифически — фагоцитами, активированными лимфокинами специфических Т-лимфоцитов. Активированные фагоциты значительно эффективнее убивают бактерии, что показал еще И. И. Мечников. Естественная невосприимчивость к возбудителям инфекционных болезней также обусловлена в основном фагоцитарными клетками. Ключевая роль принадлежит им и в детоксикации бактериальных токсинов, нейтрализованных антителами.
Макрофаги, перерабатывая антиген и представляя его лимфоцитам, участвуя в межклеточной кооперации, активации и супрессии пролиферации лимфоцитов, являются необходимым звеном в формировании иммунологической толерантности (см. Толерантность иммунологическая) и трансплантационного иммунитета (см. Иммунитет трансплантационный). Макрофаги участвуют в противоопухолевом иммунитете (см. Иммунитет противоопухолевый), оказывая цитостатическое и цитотоксическое действие на опухолевые клетки.
Повреждения фагоцитов различными иммуносупрессорами, блокаторами (см. Иммунитет, Иммунодепрессивные вещества), ионизирующим излучением (см.) вызывают резкое подавление противомикробной устойчивости организма. При воздействии на животных большими дозами ионизирующего излучения фагоцитарная активность может практически исчезнуть. Нормализуется фагоцитарная активность у животных, как правило, после 20-го дня. У кроликов, облученных в дозе 600 рад (6 Гр), она восстанавливается только через 40 дней. Между дозой ионизирующего излучения и степенью подавления фагоцитоза существует корреляция. Дозы 10—75 рад (0,1 — 0,75 Гр) усиливают фагоцитоз гранулоцитов, а 350—600 рад (3,5—6 Гр)—резко его угнетают, причем снижается завершенность фагоцитоз, в 3—4 раза подавляется подвижность фагоцитов, а также уменьшается абсолютное их число. Эти же закономерности характерны для макрофагов, число и переваривающая способность которых при облучении также резко снижаются.
Выявлены болезни, сопровождающиеся первичными (врожденными) или вторичными (приобретенными) дефектами фагоцитоза. К ним относится так называемая хроническая гранулематозная болезнь, возникающая у детей, в фагоцитах которых из-за дефекта оксидаз нарушено образование перекисей и надперекпсей и, следовательно, процесс инактивации микробов. Сниженная способность к уничтожению бактерий выявлена у людей, нейтрофилы которых синтезируют недостаточное количество миелопероксидазы, глюкозо-б-фосфат-дегидрогеназы, пируваткиназы. Замедленная гибель микробов обнаружена у больных с синдромом Чедиака — Хигаси (см. Тромбоцитопатии), в нейтрофилах которых нарушено выделение в фагосому лизосомальных ферментов из-за дефекта системы микротрубочек. Описано нарушение процесса полимеризации актина, ведущее к замедлению поглощения частиц нейтрофилами и их подвижности. Больные с указанными дефектами фагоцитов часто страдают тяжелыми бактериальными и грибковыми инфекциями.
Первичные нарушения фагоцитоза наблюдаются и на уровне опсонинов, например, при врожденном дефиците СЗ- и С5-компонентов комплемента, который может привести к развитию рецидивирующих инфекций с поражением легких, костей, кожи.
Вторичные дефекты фагоцитоза описаны при заболеваниях соединительной ткани, почек, нарушении питания, вирусных и рецидивирующих бактериальных инфекциях.
Библиогр.: Берман В. М. и Славская E. М, Завершенный фагоцитоз, Журн. микр., эпид. и иммун., № 3, с. 8, 1958; Подопригора Г. И. и Андреев В. Н. Современные методы изучения фагоцитарной активности лейкоцитов in vitro, там же, № 1, с. 19, 1976; Храмцов А. В. и Земсков В. М. Роль плазматической мембраны в активации лизосомальных ферментов, Докл. АН СССР, т. 271, № 1, с. 241, 1983; Handbook of experimental immunology, ed. by D. M. Weir, v. 2—3, Oxford a. o., 1979; Handbook of experimental pharmacology, ed. by J. R. Vane a. S. H. Ferreira, v. 50, pt 1, В. a. o., 1978; Klebanoff S. J. a. Clark R. A. The neutrophil, function and clinical disorders, Amsterdam a. o., 1978; Mononuclear phagocytes, Functional aspects, ed. by R. van Furth, pt 1 — 2, Hague a. o., 1980; The reticuloendothelial system, a comprehensive treatise, v. 1 — Morphology, ed. by H. Friedman a. o., N. Y.— L., 1980.



